Βασιλεία Αγγέλου κτηνίατρος, MSc, Δήμητρα Καρατζιά, Γεώργιος Καζάκος κτηνίατρος, PhD
Κλινική Ζώων Συντροφιάς, Τμήμα Κτηνιατρικής, Α.Π.Θ., Θεσσαλονίκη
MeSH keywords:
conscious sedation, dog, gastric dilatation, neoplasms
Περίληψη
Η αναφυλαξία είναι μια σοβαρή, απειλητική για τη ζωή αντίδραση υπερευαισθησίας, η οποία μπορεί να προκληθεί από έκθεση σε διάφορα αντιγόνα. Στην αναφυλαξία απελευθερώνονται μεσολαβητές της φλεγμονής, με αποτέλεσμα την εμφάνιση κλινικών συμπτωμάτων. Στην κτηνιατρική πράξη, στα ζώα συντροφιάς τα σημαντικότερα συμπτώματα αφορούν κυρίως στο δέρμα, στον γαστρεντερικό σωλήνα, στο κυκλοφορικό σύστημα, στο αναπνευστικό σύστημα, στο νευρικό σύστημα και στους οφθαλμούς. Η ποικιλία των συμπτωμάτων εξαρτάται από την οδό έκθεσης στο αντιγόνο και από την ταχύτητα εμφάνισής τους. Η διάγνωση της αναφυλαξίας δε βασίζεται τόσο σε εργαστηριακές μεθόδους όσο στην προσεκτική παρατήρηση των συμπτωμάτων και την λεπτομερή εξέταση του ιστορικού, το οποίο θα βοηθήσει και στον εντοπισμό του αιτιολογικού παράγοντα. Ωστόσο, η διαπίστωση του τελευταίου κατά την περιεγχειρητική περίοδο είναι δύσκολη (π.χ. λόγω των συνδυασμών των φαρμάκων που χορηγούνται). Η επείγουσα αντιμετώπιση συχνά βασίζεται στην έγκαιρη χορήγηση αδρεναλίνης, στη σωστή δόση και από τη σωστή οδό χορήγησης. Επιπλέον, η υποστηρικτική θεραπεία μπορεί να περιλαμβάνει τη χορήγηση αντιιστα μινικών, κορτικοστεροειδών και βρογχοδιασταλτικών, ενώ το οξυγόνο και τα υγρά ενδοφλεβίως είναι απαραίτητη θεραπεία όταν έχει εγκατασταθεί αναφυλακτικό σοκ. Η πρόγνωση εξαρτάται από τα κλινικά συμπτώματα και το χρονικό διάστημα που μεσολαβεί από την εμφάνισή τους έως την έναρξη της θεραπείας. Η πρόληψη δεν είναι μόνο δύσκολη, αλλά και ανέφικτη κλινικά και βασίζεται μόνο στην αποφυγή των αλλεργιογόνων. Αν και η γενικευμένη αναφυλακτική αντίδραση μπορεί να αποβεί μοιραία ακόμη και μέσα σε λίγα λεπτά, οι μελέτες σε αυτό το θέμα είναι ελάχιστες. Έτσι η διαχείριση της γενικευμένης αναφυλα κτικής αντίδρασης αποτελεί ακόμα και σήμερα πρόκληση για τον κλινικό κτηνίατρο.
Εισαγωγή
Αναφυλαξία είναι μια σοβαρή και δυνητικά απειλητική για τη ζωή αντίδραση υπερευαισθησίας, η οποία συμβαίνει αιφνίδια ύστερα από έκθεση σε κάποιο αντιγόνο (Hepner & Castells 2003, Sampson et al. 2006, Carter et al. 2011). Περιγράφηκε για πρώτη φορά το 1902 από τους Portier και Richet, οι οποίοι κατέληξαν στο συμπέρασμα ότι ο οργανισμός αρχικά ευαισθητοποιείται σε κάποιο αλλεργιογόνο και τα συμπτώματα της αναφυλαξίας εμφανίζονται όταν επανεκτεθεί στο ίδιο αλλεργιογόνο (Portier & Richet 1902). Οι κύριες κλινικές εκδηλώσεις, τόσο στην ιατρική του ανθρώπου όσο και στην κτηνιατρική, περιλαμβάνουν συμπτώματα που προέρχονται από διαφορετικά συστήματα και κυρίως από το δέρμα, το πεπτικό, το κυκλοφορικό, το αναπνευστικό, και λιγότερο συχνά από το νευρικό σύστημα και τους οφθαλμούς (Hepner & Castells 2003, Dowling 2014). Παρόλο που φαίνεται να εκδηλώνεται συχνά στον σκύλο και τη γάτα, όταν έγινε αναζήτηση στην ηλεκτρονική βάση δεδομένων PubΜed με λέξεις κλειδιά “anaphylaxis, dogs, cats” βρέθηκαν μόνο 56 δημοσιεύσεις. Οι περισσότερες από αυτές αφορούν αναφυλακτική αντίδραση σε εμβόλια, περιβαλλοντικούς παράγοντες, δήγματα εντόμων αλλά και αναισθητικά φάρμακα, αντιβιοτικά κ.ά., ενώ όταν χρησιμοποιήθηκαν ως λέξεις κλειδιά “anaphylaxis, anesthesia, dogs” οι δημοσιεύσεις κλινικών περιστατικών μειώθηκαν στις 18 συνολικά. Ειδικά κατά την περιεγχειρητική περίοδο κατά την οποία χορηγούνται πολλά φάρμακα, μπορεί να είναι δύσκολο να συσχετιστεί μία αντίδραση με ένα συγκεκριμένο φάρμακο και μάλιστα με τέτοια βεβαιότητα ώστε αυτή να μπορεί να δημοσιευτεί σε έγκυρο περιοδικό (Armitage-Chan 2010, Dowling 2014). Γενικά, τόσο στην κτηνιατρική όσο και στην ιατρική, παρά τα ποικίλα και σοβαρά συμπτώματα που μπορεί να προκύψουν από την αναφυλαξία σε πολλά και διαφορετικά συστήματα, η οριστική διάγνωση της αναφυλακτικής αντίδρασης αποτελεί πρόκληση. Για αυτόν το λόγο, τις τελευταίες δεκαετίες γίνεται προσπάθεια να καθοριστούν συγκεκριμένα και σαφή κριτήρια που θα αφορούν σε κάθε πιθανό επεισόδιο (Sampson et al. 2006, Shmuel & Cortes 2013). Η διαχείριση αυτών των περιστατικών είναι ακόμα πιο δύσκολη όταν καταλήγουν σε επιπλοκές κατά την περιεγχειρητική περίοδο.
Ο στόχος της παρούσας μελέτης είναι η βιβλιογραφική ανασκόπηση της αναφυλαξίας στον σκύλο και τη γάτα, εστιάζοντας στην παθοφυσιολογία, την αιτιολογία, τις κλινικές εκδηλώσεις, τη διάγνωση και θεραπεία, με έμφαση στην περιεγχειρητική περίοδο.
Παθογένεια
Οι αντιδράσεις υπερευαισθησίας τυπικά διαβαθμίζονται σε τέσσερεις κατηγορίες: τύπου Ι ή άμεση διαμεσολαβούμενη από IgE ανοσοσφαιρίνες, τύπου ΙΙ ή κυτταροτοξική διαμεσολαβούμενη από IgG και IgM ανοσοσφαιρίνες, τύπου ΙΙΙ που προκαλείται από το σχηματισμό ανοσοσυμπλόκων (αντιγόνου - αντισώματος) και τύπου ΙV ή καθυστερημένου τύπου διαμεσολαβούμενη από Τ-λεμφοκύτταρα (Dowling 2014).
Παρότι η αναφυλαξία έχει αποδοθεί στην τύπου Ι αντίδραση υπερευαισθησίας, έχει διαπιστωθεί και μη ανοσολογική μορφή αναφυλαξίας, τόσο στον άνθρωπο όσο και στα ζώα συντροφιάς (Ευρωπαϊκή Ακαδημία Αλλεργιολογίας και Κλινικής Ανοσολογίας). Αυτή η μορφή υπερευαισθησίας έχει ονομαστεί αναφυλακτοειδής αντίδραση, δε διαμεσολαβείται από IgE ανοσοσφαιρίνες και δεν χρειάζεται προηγούμενη έκθεση στον αιτιολογικό παράγοντα για την πυροδότησή της (Armitage-Chan 2010, Shmuel & Cortes 2013, Dowling 2014). Αυτός ο όρος δεν είναι απολύτως ακριβής, καθώς υποδοχείς IgE μπορεί να ενεργοποιηθούν από διαφορετικό αντιγόνο από εκείνο που οδήγησε στην εκδήλωση κλινικών συμπτωμάτων κατά τη διάρκεια του πρώτου αναφυλακτικού επεισοδίου (Armitage-Chan 2010). Όπως αναφέρθηκε προηγουμένως, η παθογένεια της μη ανοσολογικής αναφυλακτοειδούς αντίδρασης δεν έχει ακόμα αποσαφηνιστεί. Η παρατήρηση πως συχνά προκαλείται από ενδοφλέβια χορήγηση φαρμάκων και μάλιστα με κλινικές εκδηλώσεις ανάλογες με την ποσότητα και την ταχύτητα της έγχυσης, οδήγησε στην αποκάλυψη πως μπορεί να προκληθεί ακόμα και από μεταβολές στη διαμεμβρανική συγκέντρωση ιόντων ή μεταβολές ωσμωτικότητας ή/και διέγερση υποδοχέων, οι οποίοι έμμεσα προκαλούν έκλυση ισταμίνης (Descotes et al. 2007, Armitage-Chan 2010). Από την άλλη, οι δύο αυτές μορφές δε μπορούν να διαφοροποιηθούν κλινικά (Descotes et al. 2007, Armitage-Chan 2010). Ωστόσο, η αναφυλακτική αντίδραση είτε ανοσολογική/αλλεργική ή μη ανοσολογική/μη αλλεργική, έχει ως αποτέλεσμα την ενεργοποίηση σιτευτικών κυττάρων, την απελευθέρωση βασίφιλων κυττάρων στη συστηματική κυκλοφορία και την απελευθέρωση χημικών μεσολαβητών αναφυλαξίας, με κυριότερους την ισταμίνη, τα λευκοτριένια, τον παράγοντα ενεργοποίησης των αιμοπεταλίων (PAF), και την προσταγλανδίνη D2 (PGD2) (Hepner & Castells 2003, Peavy & Metcalfe 2008, Khan & Kemp 2011, Shmuel & Cortes 2013, Dowling 2014). Η απελευθέρωση αυτών των μεσολαβητών της φλεγμονής γίνεται σε δευτερόλεπτα έως λεπτά και η σύνθεση κυτταροκινών ξεκινά εντός ωρών (Dowling 2014). Τέλος, παραμένει άγνωστο αν η κυτταροτοξικού τύπου αντίδραση (τύπου ΙΙ), η αντίδραση με σχηματισμό ανοσοσυμπλόκων (τύπου ΙΙΙ) ή η καθυστερημένου τύπου αντίδραση υπερευαισθησίας με μεσολαβητές τα Τ-λεμφοκύτταρα (τύπου IV) μπορούν να οδηγήσουν σε αναφυλαξία (Dowling 2014).
Αιτιολογία
Γενικά οποιοσδήποτε παράγοντας μπορεί να ενεργοποιήσει τα σιτευτικά και τα βασίφιλα κύτταρα και να προκαλέσει αναφυλαξία (Hepner & Castells 2003, Simons 2009). Στους κυριότερους παράγοντες που μπορεί να προκαλέσουν αναφυλαξία συμπεριλαμβάνονται τρόφιμα, δήγματα φιδιών ή εντόμων, εμβολιασμοί καθώς και περιβαλλοντικοί παράγοντες, όπως έντονη άσκηση, έντονο ψύχος ή ζέστη (Jackson et al. 2003, Shmuel & Cortes 2013, Dowling 2014). Στα ζώα όπως και στον άνθρωπο τα φάρμακα αποτελούν μία μεγάλη κατηγορία παραγόντων υπεύθυνων για την πρόκληση αναφυλαξίας. Τα περισσότερα από αυτά είναι φάρμακα που χορηγούνται κατά την περιεγχειρητική περίοδο (π.χ. μη στεροειδή αντιφλεγμονώδη φάρμακα, αντιβιοτικά και κορτικοστεροειδή) (Schaer et al. 2005, Dowling 2014). Τα αναισθητικά φάρμακα επίσης αποτελούν συχνό αίτιο πρόκλησης είτε ανοσολογικού είτε μη ανοσολογικού τύπου αναφυλαξίας (Armitage-Chan 2010). Φάρμακα όπως η μορφίνη και η πεθιδίνη είναι γνωστό ότι προκαλούν απελευθέρωση ισταμίνης, ιδιαιτέρως κατά την ενδοφλέβια χορήγησή τους, για αυτό και δεν προτείνεται αυτή η οδός χορήγησης (Armitage-Chan 2010). Στον σκύλο και στη γάτα έχει αναφερθεί αναφυλαξία από πεντοθάλη (Mason 1976, Burren & Manson 1986), ακετυλοπρομαζίνη (Meyer 1997), ξυλαζίνη-κεταμίνη (Raptopoulos et al. 1993), αλφαξαλόνη (Haworth et al. 2019), πεθιδίνη (Schachter 1952), μεδετομιδίνη (Viscasillas et al. 2011), ελεύθερη μορφίνη και ροπιβακαΐνη ύστερα από επισκληρίδεια έγχυση (Threlfall et al. 2012), καθώς και από ροκουρόνιο (Küls et al. 2016), παραμαγνητικά σκιαγραφικά (Pollard & Pascoe 2008, Girard & Leece 2010), καθώς και άλλα φάρμακα χορηγούμενα στην περιεγχειρητική περίοδο. Άλλα αίτια είναι η μετάγγιση φρέσκου αίματος ή παραγώγων του, η χορήγηση ανθρώπινης αλβουμίνης, η χορήγηση κολλοειδών διαλυμάτων και η χρήση χημειοθεραπευτικών φαρμάκων όπως η L-ασπαργινάση (Mertes & Laxenaire 2004, Mathews 2006, Francis et al. 2007, Blake et al. 2016). Επίσης αξιοσημείωτη είναι η αναφυλακτοειδής αντίδραση από ενδοφλέβια έγχυση βιταμίνης Κ1 (Mi et al. 2014). Υπάρχουν αναπάντητα ερωτήματα για τη χρήση μυοχαλαρωτικών φαρμάκων στα ζώα συντροφιάς που έχουν ενοχοποιηθεί για αναφυλακτοειδείς αντιδράσεις στον άνθρωπο κατά τη διάρκεια της αναισθησίας. Ωστόσο, στα ζώα δεν υπάρχουν αρκετές δημοσιεύσεις ώστε να εξαχθούν συμπεράσματα, με εξαίρεση ένα περιστατικό σκύλου που εμφάνισε αναφυλακτοειδή αντίδραση κατά τη διάρκεια αναισθησίας, εξαιτίας ενδοφλέβιας χορήγησης ροκουρόνιου (Küls et al. 2016). Παρόλο που τα μυοχαλαρωτικά θεωρούνται σχετικά ασφαλή στη χρήση τους, πιθανόν λόγω της έλλειψης δημοσιεύσεων ως προς το αντίθετο, θα πρέπει να δίνεται ιδιαίτερη προσοχή ειδικά σε ζώα με ιστορικό αναφυλακτικής αντίδρασης (Jones 1992, Küls et al. 2016). Επιπλέον, έχει αναφερθεί διεγχειρητική αναφυλαξία σε περιστατικό λοβεκτομής πνεύμονα σκύλου με διροφιλαρίωση, πιθανόν λόγω τυχαίας διατομής του παρασίτου (Carter et al. 2011). Το μεγαλύτερο πρόβλημα κατά την περιεγχειρητική περίοδο με τα αναισθητικά, τα αντιβιοτικά, τα αναλγητικά και άλλα φάρμακα είναι ότι χορηγούνται σε διάφορους συνδυασμούς. Επομένως, είναι δύσκολη η ταυτοποίηση της υπεύθυνης φαρμακευτικής ουσίας και συνεπώς τα δημοσιευμένα κλινικά περιστατικά σχετικά με το θέμα αυτό είναι σπάνια (Armitage-Chan 2010). Είναι επίσης αξιοσημείωτο ότι υπάρχουν περιπτώσεις αναφυλαξίας, οι οποίες δε μπορούν να συσχετιστούν με γνωστό αιτιολογικό παράγοντα ή γεγονός (Choo et al. 2010).
Κλινικές εκδηλώσεις
Τα κλινικά συμπτώματα εξαρτώνται από το είδος του ζώου, την προηγούμενη ευαισθητοποίησή του σε αλλεργιογόνο, την ποσότητα του αλλεργιογόνου και την οδό έκθεσης στο αλλεργιογόνο (Schaer et al. 2005, Shmuel & Cortes 2013). Στην κλινική πράξη, οι σκύλοι προσκομίζονται συχνότερα με υπόταση και αιμορραγική διάρροια, ενώ συμπτώματα από το αναπνευστικό σύστημα είναι λιγότερο συχνά (Quantz et al. 2009, Shmuel & Cortes 2013). Στις γάτες, παρόλο που τα δημοσιευμένα περιστατικά είναι ελάχιστα, η κυριότερη εκδήλωση της αναφυλαξίας είναι η αναπνευστική δυσχέρεια (Litster & Atwell 2006, Moore et al. 2007, Hume-Smith et al. 2011, Dowling 2014). Τα μη εντερικά συμπτώματα εκδηλώνονται αιφνιδίως και συνήθως είναι σοβαρότερα συγκριτικά με τοπική έκθεση στο δέρμα, και περιλαμβάνουν κυρίως εκδηλώσεις από το κυκλοφορικό και το αναπνευστικό σύστημα (Schaer et al. 2005, Kemp et al. 2008). Κατόπιν εισπνοής του υπεύθυνου αλλεργιογόνου, κυρίως επηρεάζεται το έντερο, σε συνδυασμό με δερματικές αντιδράσεις και βρογχόσπασμο καθώς και εκδηλώσεις από το ρινικό βλεννογόνο (Dowling 2014). Η τοπική επαφή του αλλεργιογόνου με το δέρμα εξωτερικά μπορεί να οδηγήσει σε δερματικά και συστηματικά συμπτώματα (Dowling 2014). Η ταχύτητα με την οποία χορηγείται το υπεύθυνο αλλεργιογόνο έχει επίσης σημασία, καθώς και αν το αλλεργιογόνο έχει υποστεί αραίωση (Schaer et al. 2005, Guedes et al. 2006, Armitage-Chan 2010). Το χρονικό διάστημα που μεσολαβεί μεταξύ της έκθεσης στο αλλεργιογόνο και της έναρξης των συμπτωμάτων έχει συσχετιστεί με τη σοβαρότητα της αναφυλαξίας, τόσο στον άνθρωπο όσο και στα μικρά ζώα (Khan & Kemp 2011, Shmuel & Cortes 2013, Dowling 2014). Όσο πιο αιφνίδια είναι η εμφάνιση των συμπτωμάτων, τόσο αυξάνεται και η σοβαρότητά τους (Kemp et al. 2008, Khan & Kemp 2011). Τα συμπτώματα συνήθως εκδηλώνονται σε διάστημα 5-30 λεπτών, σε ορισμένες όμως περιπτώσεις μεσολαβούν αρκετές ώρες μέχρι την εκδήλωσή τους (Choo et al. 2010, Moore & HogenEsch 2010, Khan & Kemp 2011). Στον άνθρωπο αναφέρεται διφασική αντίδραση κατά την οποία ύστερα από την υποχώρηση των αρχικών συμπτωμάτων αυτά μπορεί να επανεμφανιστούν μέσα σε 1 έως και 72 ώρες (Sampson et al. 2006, Simons et al. 2011). Εκτός από διφασική αναφυλαξία, έχει παρατηρηθεί στον σκύλο και καθυστερημένη υπερευαισθησία τύπου ΙΙΙ με εμφάνιση συμπτωμάτων ημέρες έως εβδομάδες μετά την έκθεση στο αλλεργιογόνο (Francis et al. 2007). Συγκεκριμένα, υπάρχει δημοσίευση που αφορά στην ενδοφλέβια χορήγηση ανθρώπινης αλβουμίνης σε 6 σκύλους οι οποίοι εκδήλωσαν συμπτώματα ύστερα από 5-13 ημέρες (Francis et al. 2007) και μια άλλη που αφορά περιστατικό σκύλου που εμφάνισε συμπτώματα την τρίτη ημέρα ύστερα από χορήγηση αντιοφικού ορού (Berdoulay et al. 2005).
Τα συμπτώματα (Πίνακας 1) συνήθως προέρχονται από το δέρμα, το πεπτικό (επικρατούν στους σκύλους), το καρδιαγγειακό, το αναπνευστικό (επικρατούν στις γάτες), το νευρικό σύστημα και τους οφθαλμούς (Shmuel & Cortes 2013, Dowling 2014). Οι εκδηλώσεις από το δέρμα δεν είναι τόσο συχνές στον σκύλο και τη γάτα όσο είναι στον άνθρωπο. Μπορεί να αποτελούν μέρος του αρχικού σταδίου της εκδήλωσης της αναφυλαξίας και μπορεί να συμπεριλαμβάνονται σε καθυστερημένου τύπου αντίδραση ή μπορεί και να μην εμφανιστούν καθόλου (Sampson et al. 2006, Quantz et al. 2009). Τα δερματολογικά συμπτώματα συχνά μπορεί να είναι πολύ ήπια ή μπορεί να μην γίνουν αντιληπτά λόγω του τριχώματος ή λόγω του χρωματισμού του δέρματος (Quantz et al. 2009). Σε αυτά συμπεριλαμβάνονται το ερύθημα, ο κνησμός, η κνίδωση και το αγγειογενές οίδημα, το οποίο είναι και το συχνότερα παρατηρούμενο σύμπτωμα της αναφυλαξίας στο δέρμα και επικρατεί στον σκύλο (Armitage-Chan 2010, Shmuel & Cortes 2013, Dowling 2014). Ο κνησμός είναι συνήθως γενικευμένος, ενώ το αγγειογενές οίδημα παρατηρείται συνηθέστερα στην κεφαλή, τα άκρα και την περιοχή των γεννητικών οργάνων (Francis et al. 2007, Girard & Leece 2010, Dowling 2014).
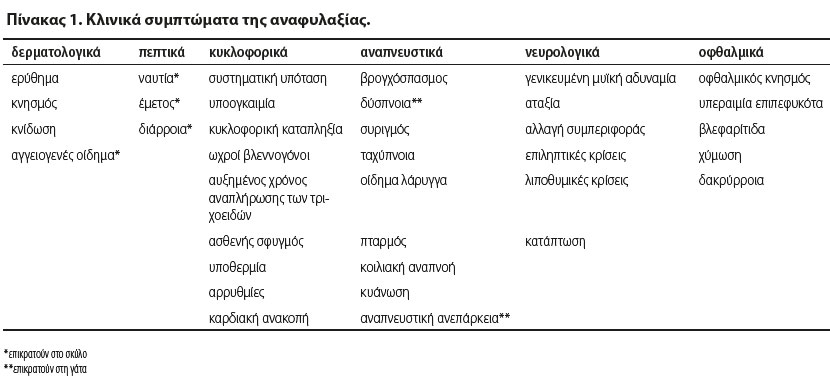
Τα συμπτώματα από το πεπτικό σύστημα είναι μη ειδικά και σε αυτά περιλαμβάνονται η ναυτία, ο έμετος και η διάρροια (Shmuel & Cortes 2013, Dowling 2014). Στον σκύλο επικρατούν τα συμπτώματα από το πεπτικό σύστημα και συχνά προκαλούνται από πυλαία υπέρταση (Lautt & Legare 1987, Richardson & Withrington 1987, Quantz et al. 2009). Υπάρχει δημοσίευση η οποία αναφέρει ότι η αυξημένη αλανινική αμινοτρανσφεράση και η μη φυσιολογική εικόνα της χοληδόχου κύστης στο υπερηχογράφημα κοιλίας σχετίζονται με αναφυλαξία (Quantz et al. 2009).
Tο κύριο σύμπτωμα κυκλοφορικής προσβολής στον σκύλο και τη γάτα είναι η υπόταση λόγω της περιφερικής αγγειοδιαστολής και της αυξημένης διαπερατότητας του τοιχώματος των αγγείων που προκαλούνται από τους μεσολαβητές της φλεγμονής κατά τη διάρκεια της αναφυλαξίας. Η αυξημένη διαπερατότητα του τοιχώματος των αγγείων οδηγεί επίσης σε εξαγγείωση υγρών από τον ενδοαγγειακό στον εξωαγγειακό χώρο με αποτέλεσμα την υποογκαιμία. Αν αυτά παραταθούν, μπορεί να οδηγήσουν σε κυκλοφορική καταπληξία (σοκ), η οποία επιπλέον χαρακτηρίζεται από ωχρούς βλεννογόνους, αυξημένο χρόνο αναπλήρωσης των τριχοειδών, ασθενή σφυγμό και υποθερμία. Εξαιτίας της υποογκαιμίας αναμένεται ταχυκαρδία, ωστόσο ενίοτε εμφανίζεται βραδυκαρδία λόγω διέγερσης του αντανακλαστικού Bezold-Jarich, το οποίο ενεργοποιείται σε περιπτώσεις υποογκαιμίας (Armitage-Chan 2010). Επιπλέον, μπορεί να εμφανιστούν αρρυθμίες ή ακόμα και καρδιακή ανακοπή (Shmuel & Cortes 2013).
Στα κύρια αναπνευστικά συμπτώματα στα μικρά ζώα συμπεριλαμβάνονται ο βρογχόσπασμος, η δύσπνοια, ο βήχας, ο συριγμός και η ταχύπνοια (Armitage-Chan 2010, Shmuel & Cortes 2013, Dowling 2014). Επιπλέον, μπορεί να υπάρχει οίδημα του λάρυγγα, πταρμός και σε σοβαρές περιπτώσεις κοιλιακού τύπου αναπνοή, κυάνωση και αναπνευστική ανεπάρκεια (Shmuel & Cortes 2013, Dowling 2014). Στις γάτες η δύσπνοια είναι το πρώτο σύμπτωμα της αναφυλαξίας, η οποία μπορεί να προέρχεται από οίδημα του λάρυγγα και του φάρυγγα, βρογχόσπασμο και αυξημένη έκκριση βλέννης (Hume-Smith et al. 2011, Dowling 2014). Στον άνθρωπο, ασθενείς με ιστορικό αναπνευστικού νοσήματος μπορεί να εκδηλώσουν εντονότερα τα αναπνευστικά συμπτώματα, ωστόσο δεν έχει αποδειχθεί ότι αυτές οι ομάδες ασθενών είναι πιο ευπαθείς ως προς την εκδήλωση αναφυλαξίας (Shmuel & Cortes 2013).
Τα νευρολογικά και οφθαλμικά συμπτώματα είναι σπανιότερα στην κλινική πράξη συγκριτικά με τα υπόλοιπα συμπτώματα που περιγράφηκαν παραπάνω. Τα νευρολογικά συμπτώματα στα μικρά ζώα περιλαμβάνουν γενικευμένη μυϊκή αδυναμία, αταξία, μεταβολές συμπεριφοράς, απώλεια συνείδησης και κατάπτωση, που σχετίζονται με την υπόταση (Quantz 2009, Hume-Smith et al. 2011, Shmuel & Cortes 2013, Dowling 2014, Rostaher et al. 2017). Τα οφθαλμικά συμπτώματα στον σκύλο και τη γάτα μπορεί να περιλαμβάνουν οφθαλμικό κνησμό, υπεραιμία του επιπεφυκότα, βλεφαρίτιδα, χύμωση και δακρύρροια (Hume-Smith et al. 2011, Shmuel & Cortes 2013).
Διάγνωση
Η κλινική διάγνωση της αναφυλαξίας αποτελεί πρόκληση, όχι μόνο λόγω της έλλειψης ειδικών παθογνωμονικών συμπτωμάτων, αλλά επίσης εξαιτίας του μεγάλου φάσματος των κλινικών εκδηλώσεων (Shmuel & Cortes 2013). Στον άνθρωπο έχουν τεθεί κριτήρια για διαγνωσθεί αναφυλαξία (Sampson et al. 2006). Ωστόσο, απαιτούνται περαιτέρω έρευνες για τη χρήση τέτοιων κριτηρίων στην κτηνιατρική (Shmuel & Cortes 2013). Στην κλινική πράξη, στα μικρά ζώα πολύ χρήσιμες μπορεί να φανούν πληροφορίες από το ιστορικό, όπως προηγούμενη αντίδραση σε εμβολιασμούς, κατανάλωση τροφίμων, νύγματα εντόμων, καθώς και πρόσφατες μεταγγίσεις ή χορήγηση αντιβιοτικών, αναισθητικών και άλλων φαρμάκων, καθώς και ο χρόνος που μεσολάβησε μεταξύ της έκθεσης σε γνωστό αντιγόνο και της εμφάνισης των συμπτωμάτων (Shmuel & Cortes 2013). Αυτές οι πληροφορίες σε συνδυασμό με την ενδεχόμενη αιφνίδια εμφάνιση των συμπτωμάτων, συχνά αποτελούν τις μοναδικές ενδείξεις αναφυλαξίας (Sampson et al. 2006, Shmuel & Cortes 2013). Αλλεργικές δοκιμές με ενδοδερμική έγχυση διαφόρων παραγόντων έχουν χαμηλή ευαισθησία και ειδικότητα, και σε περιπτώσεις που χρειάζεται άμεση θεραπευτική αντιμετώπιση όπως κατά την περιεγχειρητική περίοδο, τέτοιες δοκιμές δεν έχουν πρακτική αξία (Armitage-Chan 2010). Μέτρηση των επιπέδων της τρυπτάσης και της ισταμίνης στο αίμα γίνεται στον άνθρωπο για τη διάγνωση της αναφυλαξίας (Sampson et al. 2006, Khan & Kemp 2011). Στα ζώα συντροφιάς έχουν περιορισμένη εφαρμογή, μάλλον λόγω του περιορισμένου χρονικού διαστήματος στο οποίο πρέπει να μετρηθούν. Επομένως, είναι μη πρακτικές σε επείγοντα περιστατικά, καθώς δεν υπάρχουν αποδείξεις για τη χρησιμότητά τους στα ζώα συντροφιάς (Sampson et al. 2006, Schwartz 2006, Quantz et al. 2009, Mi et al. 2014).
Από όλα τα παραπάνω, συμπεραίνουμε ότι η διάγνωση βασίζεται στο ιστορικό και τα συμπτώματα. Η χρήση άλλων διαγνωστικών εργαλείων όπως η μέτρηση των επιπέδων βιοδεικτών στο αίμα ή η ενδοδερμική δοκιμή σπάνια γίνονται λόγω χαμηλής ευαισθησίας και ειδικότητας στη διάγνωση και την πρόγνωση αναφυλακτικής αντίδρασης.
Θεραπεία
Η αναφυλαξία αποτελεί επείγουσα κατάσταση (Simons 2009, Armitage-Chan 2010, Dowling 2014). Η θεραπευτική αντιμετώπιση πρέπει να είναι άμεση και επιθετική διότι περιστατικά τα οποία μπορεί αρχικά να μη φαίνονται απειλητικά για τη ζωή του ζώου μπορεί να οδηγήσουν στον θάνατο μέσα σε λίγα λεπτά (Sampsons et al. 2006, Shmuel & Cortes 2013, Dowling 2014). Οι θεραπευτικές επιλογές που υπάρχουν για την αναφυλακτική αντίδραση (Πίνακας 2) βασίζονται στην εμπειρία του κτηνιάτρου και εξαρτώνται από τα συμπτώματα και τις προτιμήσεις του κτηνιάτρου. Συνήθως η θεραπεία ξεκινά με την απομάκρυνση ή τη διακοπή του υποτιθέμενου παράγοντα (Shmuel & Cortes 2013). Ωστόσο, όταν ένας σκύλος ή μια γάτα προσκομίζεται με αναφυλακτικό σοκ που μπορεί να οδηγήσει σε καρδιοαναπνευστική κατάρρευση, εφαρμόζονται οι οδηγίες RECOVER, οι οποίες περιλαμβάνουν την ταχεία αξιολόγηση των αεραγωγών, της αναπνοής και του κυκλοφορικού, προκειμένου να αποκλειστεί η καρδιοαναπνευστική ανακοπή (Sampson et al. 2006, Fletcher et al. 2012, Shmuel & Cortes 2013).
Το φάρμακο επιλογής είναι η αδρεναλίνη. Η αδρεναλίνη παράγεται φυσιολογικά από τη μυελώδη μοίρα των επινεφριδίων και εκκρίνεται σε καταστάσεις απειλητικές για τη ζωή του ζώου (Mink et al. 1998, Bautista et al. 2002, Mink et al. 2004, Mathews 2006, Sampson et al. 2006, Kemp et al. 2008, Simons 2009, Simons et al. 2011, Fletcher et al. 2012, Dowling 2014). Ως φάρμακο στην αντιμετώπιση της αναφυλαξίας, η αδρεναλίνη χρησιμοποιείται κυρίως για τη δράση που έχει κατά κύριο λόγο στο καρδιαγγειακό σύστημα και στις λείες μυϊκές ίνες (Shmuel & Cortes 2013) ενεργοποιώντας τους α- και β-αδρενεργικούς υποδοχείς (Gu et al. 1999). Η επίδραση που έχει στους α-αδρενεργικούς υποδοχείς προκαλεί αγγειοσύσπαση με αποτέλεσμα την αύξηση της περιφερικής αγγειακής αντίστασης, την αύξηση της αρτηριακής πίεσης και τη μείωση του οιδήματος στους αεραγωγούς (Gu et al. 1999). Η ενεργοποίηση των β-αδρενεργικών υποδοχέων έχει ως αποτέλεσμα θετική ινοτρόπο και χρονοτρόπο δράση (μέσω των β1-αδρενεργικών υποδοχέων) στο μυοκάρδιο, με αποτέλεσμα να αυξάνεται η καρδιακή παροχή (Gu et al. 1999, Kemp et al. 2008). Εκτός της διαχείρισης των καρδιαγγειακών συμπτωμάτων, η αδρεναλίνη προκαλεί βρογχοδιαστολή, καταστέλλει την απελευθέρωση των μεσολαβητών της φλεγμονής και μειώνει την κνίδωση (μέσω των β2-αδρενεργικών υποδοχέων) (Gu et al. 1999, Kemp et al. 2008, Shmuel & Cortes 2013). Οι παρενέργειες που αναφέρονται κατόπιν έγχυσης αδρεναλίνης περιλαμβάνουν ωχρούς βλεννογόνους και νευρικότητα, τα οποία είναι συνήθως ήπια και παρατηρούνται εντός λεπτών μετά τη χορήγηση. Στις πιο σοβαρές παρενέργειες περιλαμβάνεται η ισχαιμία του μυοκαρδίου, η κρίση υπέρτασης, οι κοιλιακές αρρυθμίες και το πνευμονικό οίδημα. Αυτές ωστόσο συνήθως οφείλονται σε υπερδοσία (Shmuel & Cortes 2013).
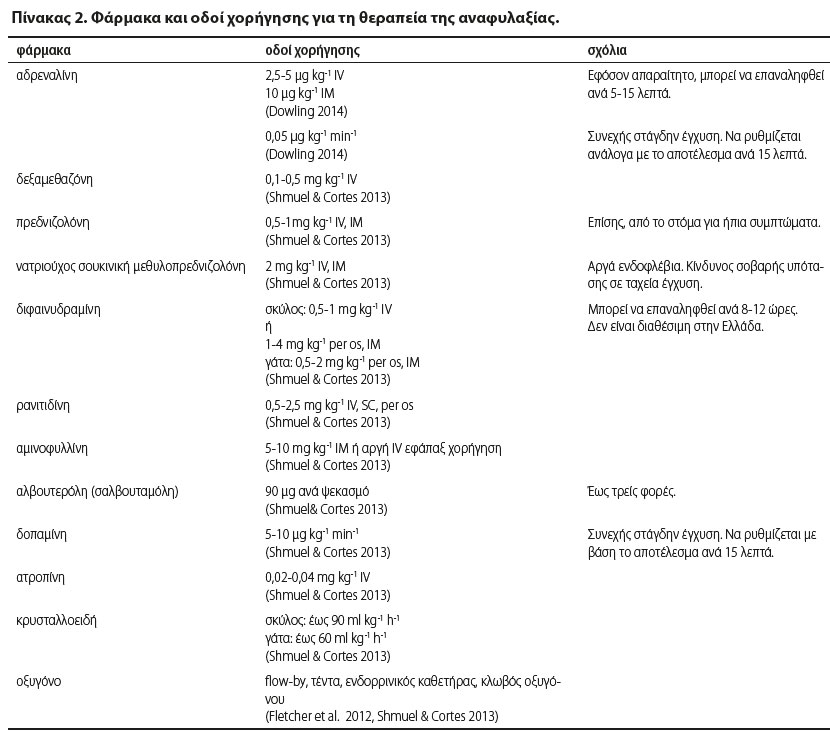
Οι προτεινόμενες δόσεις πριν εγκατασταθεί κυκλοφορική καταπληξία είναι 2,5-5 μg kg-1 kg ενδοφλεβίως (IV) από διάλυμα 1/1000 (1 mg ml-1) ή 10 μg kg-1 ενδομυϊκώς (IM) (Dowling 2014). Εφόσον χρειάζεται, μπορεί να επαναληφθεί η έγχυση ανά 5-15 λεπτά (Shmuel & Cortes 2013). Η αδρεναλίνη μπορεί να χορηγηθεί επίσης υποδορίως (SC) (Mink et al. 1998, Gu et al. 1999, Mink et al. 2004, Sampson et al. 2006, Dowling 2014), αν και αυτή η οδός χορήγησης θα πρέπει να αποφεύγεται, καθώς η απορρόφηση είναι αργή. Επιπλέον, οι χαμηλές συγκεντρώσεις αδρεναλίνης στους ιστούς μπορεί να οδηγήσουν σε αγγειοδιαστολή και να διεγείρουν την απελευθέρωση μεσολαβητών της φλεγμονής (Mink et al. 2004, Dowling 2014). Οι Mink et al. (2004) έδειξαν ότι η μέση αρτηριακή πίεση, ο όγκος παλμού, η καρδιακή παροχή και το έργο της καρδιάς ήταν πολύ μεγαλύτερα στη συνεχή στάγδην έγχυση συγκριτικά με την εφάπαξ χορήγηση. Έτσι, σε περιπτώσεις όπου το ζώο προσκομίζεται σε κατάσταση κυκλοφορικής καταπληξίας η προτεινόμενη χορήγηση είναι με συνεχή στάγδην έγχυση, με ρυθμό 0,05 μg kg-1 min-1 με ρύθμιση της δόσης αναλόγως του αποτελέσματος (Mink et al. 1998, Mink et al. 2004, Dowling 2014). Ωστόσο, άλλη αναφορά έδειξε ότι σε ζώα με εκδηλώσεις αναφυλαξίας στα οποία έχει εγκατασταθεί κυκλοφορική καταπληξία και επομένως έχει προηγηθεί η απελευθέρωση μεσολαβητών της φλεγμονής, εγχύσεις αδρεναλίνης IV, IM ή SC δεν έχουν κανένα αποτέλεσμα στην αντιστροφή της καρδιαγγειακής κατάρρευσης (Mink et al. 1998, Bautista et al. 2002, Mink et al. 2004).
Το δεύτερο επίπεδο της διαχείρισης περιλαμβάνει άλλα φάρμακα. Ωστόσο, ο ρόλος τους στη διαχείριση της αναφυλαξίας δεν έχει τεκμηριωθεί. Αυτά περιλαμβάνουν αντιισταμινικά, κορτικοστεροειδή, βρογχοδιασταλτικά, αγγειοσυσπαστικά και αντιχολινεργικά (Lautt & Legare 1987, Silverman et al. 1988, Armitage-Chan 2010, Choo et al. 2010, Dowling 2014).
Τα αντιισταμινικά χρησιμοποιούνται κατά κύριο λόγο για την αντιμετώπιση του κνησμού, της κνίδωσης και της ρινίτιδας, δηλαδή των συμπτωμάτων που προέρχονται από το δέρμα και τους βλεννογόνους και όχι τόσο για τα σοβαρά συστηματικά συμπτώματα της αναφυλαξίας (Simons et al. 2011). Γενικά χρησιμοποιούνται πρώτης γενιάς (Η1) ή δεύτερης γενιάς (Η2) αντιισταμινικά. Στα πρώτης γενιάς Η1-αντιισταμινικά συμπεριλαμβάνονται η διφαινυδραμίνη, η χλωροφαινυραμίνη, η κυπροεπταδίνη και η υδροξυζίνη (Silverman et al. 1988, Viscasillas et al. 2011, Shmuel & Cortes 2013, Dowling 2014). Θεωρούνται λιγότερο ασφαλή σε σχέση με τα δεύτερης γενιάς αντιισταμινικά και αυτό επειδή διέρχονται τον αιματοεγκεφαλικό φραγμό και μπορεί να προκαλέσουν συμπτώματα από το κεντρικό νευρικό σύστημα, όπως κόπωση, λήθαργο και γνωστική δυσλειτουργία, καθώς και συμπτώματα από το πεπτικό, όπως έμετο, διάρροια και ανορεξία (Shmuel & Cortes 2013). Τα δεύτερης γενιάς αντιισταμινικά, στα οποία περιλαμβάνονται η λορατιδίνη, η φεξοφεναδίνη και η σετιριζίνη, θεωρούνται ασφαλέστερα, ωστόσο δεν είναι εμπορικά διαθέσιμα σε μορφές για περεντερική χορήγηση. Παρόλο που τα Η2-αντιισταμινικά θεωρούνται ασφαλέστερα από τα Η1, γενικά θεωρείται ότι δεν έχουν αποτέλεσμα, τουλάχιστον μόνα τους, στην αντιμετώπιση της αναφυλαξίας, με εξαίρεση τον περιορισμό των συμπτωμάτων από το πεπτικό σύστημα (Shmuel & Cortes 2013, Dowling 2014). Γενικά για τα αντιισταμινικά δεν υπάρχουν δημοσιευμένες εργασίες που να τεκμηριώνουν όφελος από τη χρήση τους ως θεραπεία της αναφυλαξίας στα ζώα συντροφιάς. Ωστόσο, έχουν προταθεί η διφαινυδραμίνη 0,5-1 mg kg-1 IV, ενώ για χορήγηση IM ή από το στόμα, στον σκύλο συστήνεται σε δόση 1-4 mg kg-1 και στη γάτα σε δόση 0,5-2 mg kg-1. Οι χορηγήσεις μπορούν να επαναληφθούν μετά από 8-12 ώρες (Shmuel & Cortes 2013).
Τα κορτικοστεροειδή χρησιμοποιούνται ευρέως στις αλλεργικές αντιδράσεις, γεγονός που οδήγησε στην ενσωμάτωσή τους στην αντιμετώπιση της αναφυλαξίας σε βαθμό που κάποιες φορές εσφαλμένα αποτελούν φάρμακο πρώτης επιλογής, καθώς δεν υπάρχουν δημοσιεύσεις που να τεκμηριώνουν τη χρήση τους (Sampson et al. 2006, Choo et al. 2010, Girard & Leece 2010). Αποτρέπουν τον σχηματισμό αραχιδονικού οξέος και προστανοειδών, καταστέλλοντας έτσι τα συμπτώματα της καθυστερημένης αντίδρασης, ωστόσο κάτι τέτοιο δεν έχει τεκμηριωθεί (Sampson et al. 2006, Dowling 2014). Επιπλέον, τα κορτικοστεροειδή δρουν καθυστερημένα, περίπου 4-6 ώρες, ανεξάρτητα από την οδό χορήγησης, οπότε δεν έχουν αποτέλεσμα στα αρχικά στάδια της αναφυλαξίας, τα οποία μπορεί να απειλούν τη ζωή του ζώου (Shmuel & Cortes 2013, Dowling 2014). Γενικά χορηγούνται σε μία δόση εφάπαξ (Choo et al. 2010). Επιπλέον, αποτελούν κατηγορία φαρμάκων που έχει αναφερθεί πως μπορεί να προκαλέσει αναφυλαξία. Μάλιστα, υπάρχει δημοσίευση περιστατικού θανάτου σκύλου που αποδόθηκε σε αναφυλακτοειδή αντίδραση μετά τη χορη- γηση δεξαμεθαζόνης (Schaer et al. 2005). H δεξαμεθαζόνη χορηγείται σε δόση 0,1-0,5 mg kg-1 IV, η πρεδνιζολόνη σε δόση 10-25 mg kg-1 IV και η μεθυλοπρεδνιζολόνη σε δόση 30 mg kg-1 IV. Η πρεδνιζολόνη μπορεί να χορηγηθεί από το στόμα σε δόση 0,5-1 mg kg-1 προκειμένου να ελέγξει πολύ ήπια συμπτώματα (Shmuel & Cortes 2013, Dowling 2014).
Σε ορισμένα περιστατικά, είτε σε ζώα είτε στον άνθρωπο, στα οποία έχει εκδηλωθεί στο παρελθόν επεισόδιο αναφυλαξίας, συστήνεται προληπτική χορήγηση αντιισταμινικών ή κορτικοστεροειδών (Armitage-Chan 2010, Choo et al. 2010, Girard & Leece 2010). Μια τέτοια ενέργεια ωστόσο δεν αποτρέπει την εμφάνιση αναφυλαξίας, αλλά αμβλύνει τη φυσιολογική συστηματική αντίδραση του οργανισμού (Shmuel & Cortes 2013). Έτσι, παρά την ευρεία προληπτική χρήση τους στον άνθρωπο, τα αντιισταμινικά ή/και τα κορτικοστεροειδή δεν έχουν τεκμηρίωση ότι βοηθούν στην περιεγχειρητική περίοδο (Kroigaard et al. 2007, Liccardi et al. 2008).
Τα βρογχοδιασταλτικά, όπως η αλβουτερόλη και η αμινοφυλλίνη, μπορούν επίσης να χρησιμοποιηθούν, κυρίως για την αντιμετώπιση συμπτωμάτων από το αναπνευστικό. H αλβουτερόλη ανήκει στους β2-αδρενεργικούς αγωνιστές και συνήθως χορηγείται με εκνέφωση μέσω της αναπνευστικής οδού (Simons et al. 2011). Μπορεί να είναι χρήσιμη σε συμπτώματα από το κατώτερο αναπνευστικό, αλλά είναι αναποτελεσματική σε περίπτωση οιδήματος του λάρυγγα ή της τραχείας. Η αμινοφυλλίνη μπορεί επίσης να χρησιμοποιηθεί καθώς αυξάνει την ενδογενή παραγωγή αδρεναλίνης και προκαλεί χαλάρωση των λείων μυικών ινών του κατώτερου αναπνευστικού συστήματος (Shmuel & Cortes 2013). Τα βρογχοδιασταλτικά δεν αποτελούν θεραπεία πρώτης γραμμής για την αναφυλαξία και δεν αντικαθιστούν τη χρήση της αδρεναλίνης. Μπορούν να έχουν καλά αποτελέσματα μόνο στα αρχικά στάδια των συμπτωμάτων από το αναπνευστικό (Sampson et al. 2006, Shmuel & Cortes 2013, Dowling 2014). Οι προτεινόμενες δόσεις είναι για την αμινοφυλλίνη 5-10 mg kg-1 IM ή αργά IV εφάπαξ χορήγηση και για την αλβουτερόλη 90 μg ανά ψεκασμό, μέχρι τρεις φορές συνολικά (Shmuel & Cortes 2013).
Στις άλλες θεραπευτικές επιλογές συμπεριλαμβάνονται η χορήγηση αγγειοσυσπαστικών όπως είναι η δοπαμίνη, η νοραδρεναλίνη και η αντιδιουρητική ορμόνη με στόχο την αύξηση της αρτηριακής πίεσης σε υποτροπιάζουσα υπόταση (Lautt & Legare 1987, Shmuel & Cortes 2013, Dowling 2014). Η δοπαμίνη έχει δοσοεξαρτώμενη δράση και αρχικά αυξάνει τη συσπαστικότητα του μυοκαρδίου, ενώ ακολούθως προκαλεί αγγεισοσύσπαση όταν χορηγείται σε αυξημένες δόσεις, μέσω ενεργοποίησης των β1- και α1-αδρενεργικών υποδοχέων. Η νοραδρεναλίνη επίσης μπορεί να χορηγηθεί για την αγγειοσυσπαστική της δράση. Αν και η αντιδιουρητική ορμόνη δεν έχει μελετηθεί αρκετά στα ζώα, υπάρχουν αναφορές περιστατικών με έντονη υπόταση που ενώ δεν ανταποκρινόταν στη δοπαμίνη ανταποκρίθηκαν στην αντιδιουρητικη ορμόνη (Kill et al. 2004, Silverstein et al. 2007, Scroggin & Quandt 2009). Η ατροπίνη ενδείκνυται σε ασθενείς με υποτροπιάζουσα βραδυκαρδία (Dowling 2014).
Για την αντιμετώπιση της αναφυλαξίας πρωταρχικής σημασίας είναι η χορήγηση υγρών ενδοφλεβίως (Shmuel & Cortes 2013, Dowling 2014). Η προκαλούμενη διαστολή των αρτηριδίων οδηγεί σε εξαγγείωση μεγάλης ποσότητας νερού από αυτά, καθώς και συσσώρευση του αίματος, με αποτέλεσμα τη δραματική μείωση του κυκλοφορούντος όγκου αίματος (Brown 2005). Σκοπός, λοιπόν, είναι η αύξηση του ενδοαγγειακού όγκου, η αύξηση της αρτηριακής πίεσης, η αποφυγής της εγκατάστασης κυκλοφορικής καταπληξίας. Τα υγρά που μπορούν να χορηγηθούν IV είναι είτε ισότονα κρυσταλλοειδή (έως 90 ml kg-1 στον σκύλο, 60 ml kg-1 στη γάτα, συνολικά), είτε κολλοειδή (π.χ. hetastarch) σε εφάπαξ χορηγήσεις 5 ml kg-1 IV ανά έγχυση, μέχρι συνολικής ημερησίας δόσης 20 ml kg-1 για γρήγορη αποκατάσταση του κυκλοφορούντος όγκου αίματος (Shmuel & Cortes 2013, Dowling 2014).
Μεγάλης σημασίας σε αυτούς τους ασθενείς είναι η χορήγηση οξυγόνου flow-by, με τέντα, με ενδορρινικό καθετήρα ή με κλωβό οξυγόνου, ιδιαίτερα σε αυτούς με συμπτώματα από το αναπνευστικό (Armitage-Chan 2010, Shmuel & Cortes 2013, Dowling 2014).
Τέλος, στα ζώα που εκδηλώνουν σοβαρή αναφυλαξία και τα οποία προσκομίζονται σε κυκλοφορική καταπληξία θα πρέπει να εφαρμόζεται στενός έλεγχος των ζωτικών λειτουργιών και εφόσον είναι εφικτό θα πρέπει να έχουν συνεχή έλεγχο με ηλεκτροκαρδιογραφία για την αξιολόγηση του καρδιακού ρυθμού και της συχνότητας, μέτρηση της αρτηριακής πίεσης, αξιολόγηση της οξυγόνωσης και του αερισμού, αξιολόγηση του τελοεκπνευστικού CO2 και της παραγωγής ούρου, καθώς μπορεί τα περιστατικά αυτά να εκδηλώσουν διφασική αναφυλαξία με αρχική βελτίωση των συμπτωμάτων και κατόπιν υποτροπή (Fletcher et al. 2012, Shmuel & Cortes 2013). Η στενή παρακολούθηση συστήνεται για τρεις ημέρες σε περιστατικά διφασικής αναφυλαξίας, η οποία έχει αναφερθεί στον σκύλο μέχρι και 48 ώρες μετά το αρχικό επεισόδιο (Shmuel & Cortes 2013).
Επίλογος
Η περιεγχειρητική αναφυλαξία αποδίδεται σε πολλά φάρμακα συμπεριλαμβανομένων των αναισθητικών και αντιβιοτικών. Παράγοντες οι οποίοι έχουν ενοχοποιηθεί για την εκδήλωση αναφυλαξίας θα πρέπει να αποφεύγονται, όπου είναι δυνατόν (Shmuel & Cortes 2013, Dowling 2014). Σε τέτοια περιστατικά η μόνη προληπτική ενέργεια είναι η αργή έγχυση των φαρμάκων εφόσον είναι απαραίτητη η ενδοφλέβια οδός χορήγησης, ιδιαίτερα σε φάρμακα για τα οποία υπάρχουν σχετικές αναφορές (Armitage-Chan 2010). Υπάρχουν ακόμα αρκετά αναπάντητα ερωτήματα ως προς το γιατί ορισμένοι ασθενείς εκδηλώνουν ήπια συμπτώματα ενώ για άλλους η αναφυλαξία μπορεί να αποβεί θανατηφόρα, και γιατί κάποια περιστατικά παρά την έγκαιρη και επιθετική αντιμετώπιση δεν ανταποκρίνονται ενώ σε άλλα περιστατικά τα συμπτώματα μπορεί να υποχωρήσουν ακόμα και χωρίς καμία αγωγή (Armitage- Chan 2010, Shmuel & Cortes 2013). Ένα βήμα προς την καλύτερη περιγραφή του φαινομένου περιεγχειρητικά θα είναι η καταγραφή και δημοσίευση κάθε περιστατικού αναφυλαξίας.
Βιβλιογραφία
- Armitage-Chan E (2010) Anaphylaxis and anaesthesia. Vet Anaesth Analg 37, 306-310.
- Bautista E, Simons FE, Simons KJ et al. (2002) Epinephrine fails to hasten hemodynamic recovery in fully developed canine anaphylactic shock. Int Arch Allergy Immunol 128, 151-164.
- Berdoulay P, Schaer M, Starr J (2005) Serum sickness in a dog associated with antivenin therapy for snake bite caused by Crotalus adamanteus. J Vet Emerg Crit Care 15, 206-212.
- Blake MK, Carr BJ, Mauldin GE (2016) Hypersensitivity reactions associated with L-asparaginase administration in 142 dogs and 68 cats with lymphoid malignancies: 2007-2012. Can Vet J 57(2), 176- 182.
- Brown S (2005) Cardiovascular aspects of anaphylaxis: implications for treatment and diagnosis. Curr Opin Allergy Clin Immunol 5, 359-364.
- Burren VS, Manson KV (1986) Suspected anaphylaxis to thiopentone in a dog. Austral Vet J 63, 384-385.
- Carter JE, Chanoit G, Kata C (2011) Anaphylactoid reaction in a heratworm-infected dog undergoing lung lobectomy. J Am Vet Med Assoc 238, 1301-1304.
- Choo KJ, Simons FE, Sheikh A (2010) Glucocorticoids for the treatment of anaphylaxis: Cochrane systematic review. Allergy 65, 1205-1211.
- Descotes J, Payen C, Vial T (2007) Pseudo-allergic drug reactions with special reference to direct histamine release. Perspect Exp Clin Immunotoxicol 1, 41-50.
- Dowling P (2014) Anaphylaxis. In: Small Animal Critical Care Medicine. 2nd ed. Silverstein D, Hopper K. WB Saunders: St Louis, Missouri, pp. 807-810.
- Fletcher DJ, Boller M, Brainard BM et al. (2012) RECOVER evidence and knowledge gap analysis on veterinary CPR. Part 7: Clinical guidelines.J Vet Emerg Crit Care 22(s1), S102-S131.
- Francis H, Martin L, Haldorson G et al. (2007) Adverse reactions suggestive of type III hypersensitivity in six healthy dogs given human albumin. J Am Vet Med Assoc 230, 873-879.
- Girard NM, Leece EA (2010) Suspected anaphylactoid reaction following intravenous administration of a gadolinium- based contrast agent in three dogs undergoing magnetic resonance imaging. Vet Anaesth Analg 37, 352-356.
- Guedes AG, Rude EP, Rider MA (2006) Evaluation of histamine release during constant rate infusion of morphine in dogs. Vet Anaesth Analg 33, 28-35.
- Gu X, Simons FE, Simons KJ (1999) Epinephrine absorption after different routes of administration in an animal model. Biopharm Drug Dispos 20, 401-405.
- Haworth M, McEwen M, Dixon B et al. (2019) Anaphylaxis associated with intravenous administration of alphaxalone in a dog. Aust Vet J 97, 197-201.
- Hepner DL, Castells M (2003) Anaphylaxis During the Perioperative Period. Anesth Analg 97, 1381-1395.
- Hume-Smith KM, Groth AD, Rishniw M et al. (2011) Anaphylactic events observed within 4 h of ocular application of an antibioticcontaining ophthalmic preparation: 61 cats (1993-2010). J Feline Med Surg 13, 744-751.
- Jackson HA, Jackson MW, Coblentz L et al. (2003) Evaluation of the clinical and allergen specific serum immunoglobulin E responses to oral challenge with cornstarch, corn, soy and a soy hydrolysate diet in dogs with spontaneous food allergy. Vet Dermatol 14, 181–187.
- Jones RS (1992) Muscle relaxants in canine anaesthesia 1: History and the drugs. J Small Anim Pract 33, 371-375.
- Kemp SF, Lockey RF, Simons FE (2008) Epinephrine: the drug of choice for anaphylaxis: a statement of the World Allergy Organization. WHO Journal S2, S18-S26.
- Khan BQ, Kemp SF (2011) Pathophysiology of anaphylaxis. Curr Opin Allergy Clin Immunol 11, 319–325.
- Kill C, Wranze E, Wulf H (2004) Successful treatment of severe anaphylactic shock with vasopressin. Int Arch Allergy Immunol 134, 260–261.
- Kroigaard M, Garvey LH, Gillberg I et al. (2007) Scandinavian clinical practice guidelines on the diagnosis, management and follow-up of anaphylaxis during anaesthesia. Acta Anaesthesiol Scand 51(6), 655–670.
- Küls N, Rocchi A, Larenza PM (2016) Suspected anaphylaxis after intravenous injection of rocuronium in a dog. Vet Rec Case Rep 4, 1-5.
- Lautt WW, Legare DJ (1987) Effect of histamine, norepinephrine, and nerves on vascular pressures in dog liver. Am J Physiol 252, G472–G478.
- Liccardi G, Lobetalo G, Di Florio E et al. (2008) Strategies for the prevention of asthmatic, anaphylactic and anaphylactoid reactions during the administration of anesthetics and/or contrast media. J Investig Allergol Clin Immunol 18, 1–11.
- Litster A, Atwell R (2006) Physiological and haematological findings and clinical observations in a model of acute systemic anaphylaxis in Dirofilaria immitis sensitized cats. Aust Vet J 84, 151–157.
- Mason TA (1976) Anaphylactic response to thiopentone in a dog. Vet Rec 98, 136.
- Mathews KA (2006). Anaphylactic and anaphylactoid reactions. In: Veterinary Emergency and Critical Care Manual. 2nd ed. Mathews KA ed Life Learn, Ontario, Canada, pp. 615-618.
- Mertes PM, Laxenaire MC (2004) Anaphylactic and anaphylactoid reactions occurring during anaesthesia in France. Seventh epidemiologic survey (January 2001- December 2002). Ann Fr Anesth Reanim 23, 1133–1134.
- Meyer EK (1997) Rare, idiosyncratic reaction to acepromazinein dogs. J Am Vet Med Assoc 210, 1114–1115.
- Mi Y-N, Ping N-N, Xiao X et al. (2014). The Severe Adverse Reaction to Vitamin K1 Injection Is Anaphylactoid Reaction but Not Anaphylaxis. PLOS ONE 9, 1-10.
- Mink SN, Bands C, Becker A et al. (1998) Effect of bolus epinephrine on systemic hemodynamics in canine anaphylactic shock. Cardiovasc Res 40, 546–556.
- Mink SN, Simons FE, Simons KJ et al. (2004) Constant infusion of epinephrine, but not bolus treatment, improves haemodynamic recovery in anaphylactic shock in dogs. Clin Exp Allergy 34, 1776–1783.
- Moore GE, DeSantis Kerr AC, Guptiill LF et al. (2007) Adverse events after vaccine administration in cats: 2560 cats (2002-2005). J Am Vet Med Assoc 231, 94-100.
- Moore GE, HogenEsch H (2010) Adverse vaccinal events in dogs and cats. Vet Clin N Am Small Anim Pract 40, 393–407
- Peavy RD, Metcalfe DD (2008) Understanding the mechanisms of anaphylaxis. Curr Opin Allergy Clin Immunol 8, 310–315.
- Pollard RE, Pascoe PJ (2008) Severe reaction to intravenous administration of an ionic iodinated contrast agent in two anesthetized dogs. J Am Vet Med Assoc 233, 274–278.
- Portier P, Richet C (1902) De l’action anaphylactique de certains venins. C R Séances Soc Biol 54,170
- Quantz J, Miles M, Reed A et al. (2009) Elevation of alanine transaminase and gallbladder wall abnormalities as biomarkers of anaphylaxis in canine hypersensitivity patients. J Vet Emerg Crit Care 19, 536–544.
- Raptopoulos D, Papazoglou L, Galatos A (1993) Suspected adverse reaction to xylazine-ketamine anesthesia in a cat. Fel Pract 21, 27–29.
- Richardson PD, Withrington PG (1978) Responses of the simultaneously-perfused hepatic arterial and portal venous vascular beds of the dog to histamine and 5-hydroxytryptamine. Br J Pharmacol 64, 581–588.
- Rostaher A, Hofer-Inteeworn N, Kümmerle-Fraune C, Fischer NM, Favrot, C. (2017). Triggers, risk factors and clinico-pathological features of urticaria in dogs - a prospective observational study of 24 cases.Vet Dermatol 28(1), 39–46.
- Sampson HA, Munoz-Furlong A, Campbell RL et al. (2006) Second symposium on the definition and management of anaphylaxis: summary report—Second National Institute of Allergy and Infectious Disease/Food Allergy and Anaphylaxis Network Symposium. J Allergy Clin Immunol 117, 391–397.
- Schachter M (1952) The release of histamine by pethidine, atropine, quinine, and other drugs. Brit J Pharmacol 7, 646–653.
- Schaer M, Ginn PE, Hanel RM (2005) A case of fatal anaphylaxis in a dog associated with a dexamethasone suppression test. J Vet Emerg Crit Care 15, 213–216.
- Scroggin RD, Quandt J (2009) The use of vasopressin for treating vasodilatory shock and cardiopulmonary arrest. J Vet Emerg Crit Care 19, 145–157.
- Schwartz LB (2006) Diagnostic value of tryptase in anaphylaxis and mastocytosis. Immunol Allergy Clin N Am 26, 451–463.
- Shmuel D, Cortes Y (2013) Anaphylaxis in dogs and cats. J Vet Emerg Crit Care 23, 377-394.
- Silverman HJ, Taylor WR, Smith PL et al. (1988) Effects of antihistamines on the cardiopulmonary changes due to canine anaphylaxis. J Appl Physiol 64, 210–217.
- Silverstein DC, Waddell LS, Drobatz KJ et al. (2007) Vasopressin therapy in dogs with dopamine resistant hypotension and vasodilatory shock. J Vet Emerg Crit Care 17, 399–408.
- Simons FE, (2009) Anaphylaxis: Recent advances in assessment and treatment. J Allergy Clin Immunol 124, 625–636.
- Simons FE, Ardusso LR, Bilo MB et al. (2011) World allergy organization guidelines for the assessment and management of anaphylaxis. World Allergy Organ J 4, 13-37.
- Threlfall A, Viscasillas J, Volk A (2012). Localised cutaneous reaction after epidural administration of preservative free morphine and ropivacaine? Vet Anaesth Analg, 39(5), 559–560. #Viscasillas J, Seymour C, Knudsen T, Levien A, Volk A (2011). Cutaneous reaction after intravenous administration of medetomidine? Vet Anaesth Analg, 38(4), 413–414.
Υπεύθυνη αλληλογραφίας:
Βασιλεία Αγγέλου
e-mail: Αυτή η διεύθυνση ηλεκτρονικού ταχυδρομείου προστατεύεται από τους αυτοματισμούς αποστολέων ανεπιθύμητων μηνυμάτων. Χρειάζεται να ενεργοποιήσετε τη JavaScript για να μπορέσετε να τη δείτε.



