Βελτιωνόμαστε με την κατανόηση
> Περίληψη
Η χρόνια νεφρική νόσος (ΧΝΝ) της γάτας χαρακτηρίζεται από μη αναστρέψιμες δομικές αλλοιώσεις στους νεφρούς και μπορεί να εξελιχθεί σε χρόνια νεφρική ανεπάρκεια (ΧΝΑ), η οποία καταλήγει τελικά στη συσσώρευση των κατάλοιπων του μεταβολισμού και στη διαταραχή της ενυδάτωσης, των ηλεκτρολυτών και της οξεοβασικής ισορροπίας. Η ΧΝΝ προσβάλλει κυρίως τις ηλικιωμένες γάτες. Στην πλειονότητα των ζώων ο εναυσματικός παράγοντας της ΧΝΝ παραμένει ασαφής. Έχουν ενοχοποιηθεί ιδιοπαθείς, οικογενείς, συγγενείς, φλεγμονώδεις, λοιμώδεις και νεοπλασματικοί παράγοντες. Όταν πλέον έχουν εγκατασταθεί οι αλλοιώσεις, η περαιτέρω βλάβη των νεφρών «αυτοδιαιωνίζεται». Τα κυριότερα συμπτώματα είναι η ανορεξία, η απώλεια βάρους, ο έμετος και η διάρροια. Η πρώιμη διάγνωση της ΧΝΝ είναι καίριας σημασίας. Κατά τον εργαστηριακό έλεγχο μπορεί να παρατηρηθούν αναιμία, αζωθαιμία, υπερφωσφαταιμία και υποκαλιαιμία. Η ακτινογράφηση και ο υπερηχοτομογραφικός έλεγχος της κοιλιακής κοιλότητας μπορεί να συμβάλουν στην ταυτοποίηση του εναυσματικού παράγοντα. Η ιστοπαθολογική εξέταση των νεφρών μπορεί να οδηγήσει στην αιτιολογική διάγνωση. Οι συνέπειες της ΧΝΝ είναι πολυσυστηματικές και περιλαμβάνουν την αρτηριακή υπέρταση, το νεφρογενή δευτερογενή υπερπαραθυρεοειδισμό, την αναιμία, τις γαστρεντερικές επιπλοκές και τις διαταραχές της οξεοβασικής ισορροπίας και διαφόρων ηλεκτρολυτών.
> Εισαγωγή
Η χρόνια νεφρική νόσος (ΧΝΝ), η οποία μπορεί να εξελιχθεί σε χρόνια νεφρική δυσλειτουργία (ΧΝΔ) ή ανεπάρκεια (ΧΝΑ), είναι πολύ συχνή στις γάτες και αποτελεί μία από τις κύριες αιτίες θανάτου των υπερήλικων ζώων. 1-3 Η βλάβη του νεφρού συμβαίνει οποιαδήποτε στιγμή κατά τη διάρκεια της ζωής της γάτας, ωστόσο μπορεί να μην γίνει αντιληπτή έως ότου εγκατασταθεί η ΧΝΑ. Η ΧΝΑ χαρακτηρίζεται από μη αναστρέψιμες βλάβες των νεφρών, που έχουν ως αποτέλεσμα τη μείωση της δομικής και λειτουργικής τους ακεραιότητας. Η βλάβη των νεφρών οδηγεί σε απορρύθμιση των υγρών και της οξεοβασικής ισορροπίας του οργανισμού και σε μειωμένη απομάκρυνση των κατάλοιπων του μεταβολισμού. Επίσης, μπορεί να οδηγήσει σε μειωμένη παραγωγή διαφόρων ορμονών ή να αποτελεί το όργανο-δράσης για αυτές όπως η ερυθροποιητίνη, η 1,25-διυδροξυχολοκαλσιφερόλη (καλσιτριόλη), η αντιδιουρητική ορμόνη, η ρενίνη και η αλδοστερόνη. 3,4
Εξελικτικά, η νεφρική ανεπάρκεια καταλήγει σε ουραιμία. 5 Λαμβάνοντας υπόψη το βαθμό της συγκέντρωσης της κρεατινίνης στον ορό του αίματος, την πρωτεϊνουρία και την αρτηριακή υπέρταση, η International Renal Interest Society (IRIS) ανέπτυξε για τη ΧΝΝ ένα σύστημα σταδιοποίησης το οποίο περιλαμβάνει τέσσερα στάδια.2
> Αιτιολογία
Η ΧΝΝ της γάτας μπορεί να προέλθει από διάφορους παράγοντες, οι οποίοι επιδρούν άμεσα ή έμμεσα στους νεφρούς. Ανεξάρτητα από την αιτία της, όταν προκύπτει η νεφρική βλάβη, η ΧΝΝ θεωρείται μία εξελισσόμενη εκφυλιστική διαταραχή. Η νεφρική δυσλειτουργία εμφανίζεται όταν καταστραφούν περισσότερο από τα 3/4 (75%) των νεφρών. Τα συμπτώματα της ουραιμίας εμφανίζονται συνήθως όταν οι αλλοιώσεις επεκτείνονται στο 80-85% των νεφρών. 6,7
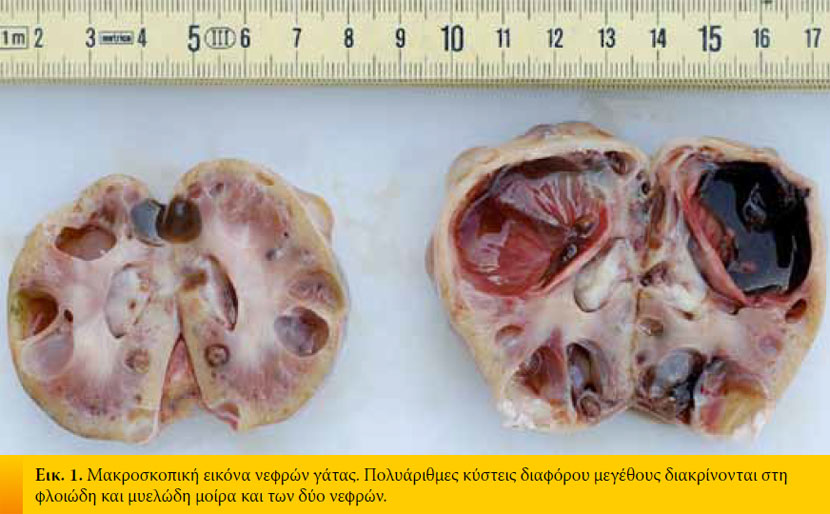
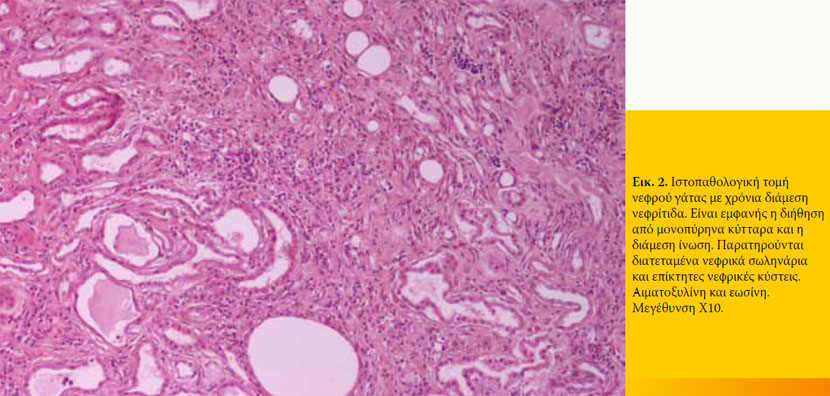
Ως αιτίες της ΧΝΝ έχουν ενοχοποιηθεί ιδιοπαθείς, συγγενείς, φλεγμονώδεις, λοιμώδεις ή νεοπλασματικοί παράγοντες. 2,3 Ωστόσο στο 50% περίπου των ασθενών γατών ο αιτιολογικός παράγοντας ήταν η ιδιοπαθής διάμεση νεφρίτιδα (Πίνακας 1). 8 Πρόσφατα, οι Lawler και συν. 1 πρότειναν ότι η ΧΝΝ της γάτας είναι ένα εκφυλιστικό φαινόμενο το οποίο αποτελεί συνέπεια της γήρανσης του οργανισμού. Επίσης, η πολυκυστική νόσος των νεφρών είναι συχνή στις γάτες Περσικής φυλής (Εικ.1). Η συχνότητα εμφάνισης της νόσου ποικίλλει γεωγραφικά για τη φυλή αυτή και φτάνει περίπου το 50% στη Μεγάλη Βρετανία και τη Γαλλία. 9,10 Παρόλο που δεν υπάρχουν δημοσιευμένες μελέτες που να αποδεικνύουν την αιτιοπαθογενετική σχέση μεταξύ της ΧΝΝ και της νεφρολιθίασης, οι Ross και συν. 11 βρήκαν πρόσφατα ότι η νεφρολιθίαση δε συσχετίζεται θετικά με την εξέλιξη της ΧΝΝ. Ορισμένα περιστατικά ΧΝΑ σε γάτες αποδόθηκαν από τους Minkus και συν. 12 σε ανοσολογικούς μηχανισμούς, λόγω της διήθησης των νεφρών από λεμφοκύτταρα και πλασμοκύτταρα, γεγονός που υποδηλώνει χρόνια διαμεσωληναριακή νεφρίτιδα (Εικ 2). Επιπλέον, οι Lappin και συν. 13 δεν κατάφεραν να συσχετίσουν τον εμβολιασμό των γατών ενάντια στον ερπητοϊό (FHV), τον καλυκοϊό (FCV), και την πανλευκοπενία (FPV) με τη ΧΝΝ. Υποτροπιάζοντα ή μη αντιμετωπίσιμα επεισόδια της νόσου του κατώτερου ουροποιητικού της γάτας, 14 μιας συχνής κλινικής οντότητας και η μόλυνση από τον ιό της επίκτητης ανοσοανεπάρκειας μπορούν τελικά να οδηγήσουν σε ΧΝΑ. Οι German και συν. 15 εικάζουν ότι ο foamy virus της γάτας, που ανήκει στους ρετροϊούς και που θεωρείται πως έχει ευρεία εξάπλωση στους πληθυσμούς των γατών, θα μπορούσε να αποτελεί την αιτία της σπειραματονεφρίτιδας που ανιχνεύεται σε γάτες μετά από πειραματική μόλυνση.
Μία ενδιαφέρουσα παθολογική κατάσταση αποτελεί η έμφραξη του ουρητήρα εξαιτίας κάποιου ουρόλιθου, ουρητηρίτιδας ή λόγω συσσώρευσης βυσμάτων, ενώ ο ρυθμός σπειραματικής διήθησης (ΡΣΔ) στον ετερόπλευρο νεφρό είναι μειωμένος εξαιτίας ΧΝΝ. Η οντότητα αυτή χαρακτηρίζεται ως ένα “οξύ επεισόδιο σε έδαφος χρόνιας” νεφρικής ανεπάρκειας. Οι γάτες προσκομίζονται με ουραιμική κρίση εξαιτίας των αλλοιώσεων της ΧΝΝ και ταυτόχρονης δυσλειτουργίας του άλλου νεφρού. Κατά την ψηλάφηση της κοιλιακής κοιλότητας ο ένας νεφρός είναι μικρός σε μέγεθος και ανώμαλος, ενώ ο άλλος είναι διογκωμένος και ίσως επώδυνος. Η οντότητα αυτή καλείται “σύνδρομο του μεγάλου και του μικρού νεφρού”. 16
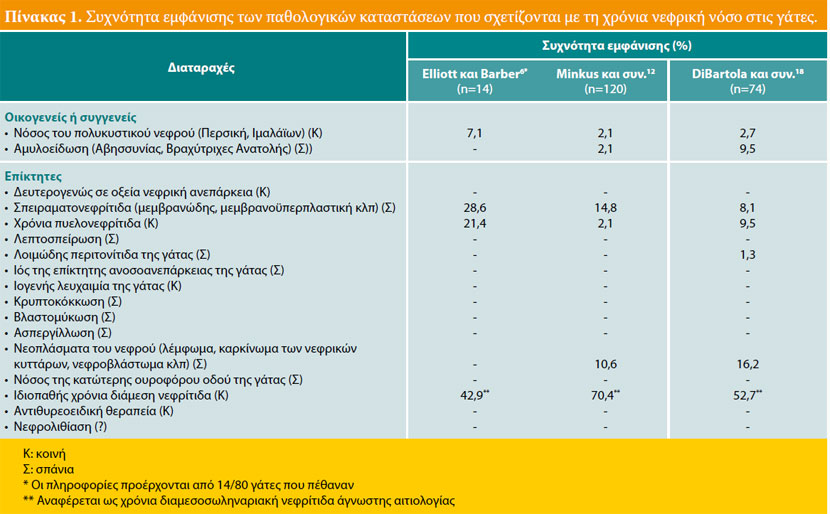
Αναφέρεται ότι η υποκείμενη αιτία αρχικά επηρεάζει το διαμεσοσωληναριακό χώρο, 7,17 σήμερα όμως η άποψη αυτή δε φαίνεται να ισχύει. Εξάλλου, οι αλλοιώσεις που εντοπίζονται σε μία συγκεκριμένη ανατομική περιοχή του νεφρού επεκτείνονται προοδευτικά και στον υπόλοιπο. 4,7,17 Στις περισσότερες γάτες με ΧΝΑ, ο αιτιολογικός παράγοντας μπορεί να μην εντοπιστεί παρά τη σωστή διαγνωστική προσέγγιση. Αυτό επιβεβαιώθηκε από διάφορες μελέτες στις οποίες ακόμη και μετά από ιστοπαθολογική εξέταση του νεφρού, δεν τέθηκε οριστική διάγνωση, 12,18 γεγονός που ίσως να αποδίδεται στη λειτουργική ανεξαρτησία διαφόρων τμημάτων των νεφρώνων, στον περιορισμό της ανταπόκρισης διαφόρων ανατομικών στοιχείων του νεφρού σε ποικίλους παράγοντες και την αδυναμία των νεφρώνων να αποκατασταθούν όταν έχουν υποστεί μη αναστρέψιμες βλάβες. Σε μία μελέτη, χρόνια διαμεσωληναριακή νεφρίτιδα ανιχνεύθηκε στο 70,4% των γατών με ΧΝΑ, ενώ μεμβρανώδης σπειραματονεφρίτιδα, νεοπλάσματα (ιδιαίτερα λέμφωμα) και αμυλοείδωση παρατηρήθηκαν σε ποσοστό 14,8%, 11%, και 2%, αντίστοιχα. 12
> Παθογένεια
Στον άνθρωπο και στο σκύλο, η ΧΝΝ χαρακτηρίζεται από προοδευτική απώλεια της νεφρικής λειτουργίας, ενώ στις γάτες μπορεί να παρατηρηθεί μία πιο απότομη (κλιμακωτή) μείωση του ΡΣΔ, με αποτέλεσμα να εμφανίζεται αιφνίδια ουραιμική κρίση σε έναν κατά τα άλλα σταθερό ασθενή. 6,19 Κατά τη διάρκεια της ΧΝΝ, πολλοί νεφρώνες καθίστανται μη λειτουργικοί. Οι βιώσιμοι νεφρώνες υπερλειτουργούν, υπερτρέφονται και υπερπλάσσονται, ώστε να επιτελούν το έργο των νεφρών. Πέραν αυτού, παρουσιάζεται και ενδοσωληναριακή υπέρταση, η οποία καταστρέφει με τη σειρά της γρήγορα τους βιώσιμους νεφρώνες. Αν και αυτό το υπερδιηθητικό στάδιο θεωρούνταν παλαιότερα ευεργετικό, τώρα πιστεύεται ότι είναι μάλλον επιζήμιο. 20,21 Η απώλεια της νεφρικής λειτουργίας αναμένεται νωρίτερα στη διαμεσοσωληναριακή νεφρίτιδα σε σχέση με τη σπειραματοπάθεια, 20 αν και το προσδόκιμο ζωής ήταν μεγαλύτερο σε γάτες με διαμεσοσωληναριακή νεφρίτιδα σε σχέση με αυτές που έπασχαν από άλλες νεφροπάθειες. 1 Επίσης, αναφέρεται ότι η πρωτεϊνουρία λόγω σπειραματοπάθειας συμβάλλει στην “εσωτερική τοξίκωση” του νεφρού και σε περαιτέρω βλάβη των νεφρώνων, αλλά ο ακριβής ρόλος της στην εξέλιξη της νεφρικής νόσου παραμένει ασαφής. 22 Αν και δεν έχει επιβεβαιωθεί στις γάτες, η βλάβη των νεφρώνων λόγω της πρωτεϊνουρίας, αποδίδεται στην καταστροφή των επιθηλιακών κυττάρων των ουροφόρων σωληναρίων, εξαιτίας της επαναρρόφησης των λευκωματινών, στην τοξίκωση από την τρανσφερίνη ή το σίδηρο ή στην επίδραση διαφόρων κυτταροκινών. 20 Είναι ακόμη αμφισβητούμενο αν η πρωτεϊνουρία αποτελεί επίπτωση ή αιτία της ΧΝΝ της γάτας. 22 Παρ’ όλα αυτά, εάν η υποκείμενη αιτία συνεχίζει να υφίσταται, αναμένεται περαιτέρω απώλεια της νεφρικής λειτουργίας 2,20 που οδηγεί με τη σειρά της σε σημαντική νεφρική βλάβη. 23 Τέλος, όταν εγκατασταθεί η νεφρική ανεπάρκεια, οι επιπτώσεις της δεν επηρεάζουν μόνο τα διάφορα όργανα του οργανισμού, αλλά με άμεσο ή έμμεσο τρόπο και τους ίδιους τους νεφρούς, επιδεινώνοντας την ήδη υφιστάμενη βλάβη. 24
> Διαγνωστική προσέγγιση
Η διαγνωστική προσέγγιση της ΧΝΝ της γάτας θα πρέπει να στοχεύει, εάν είναι δυνατόν, στην ταυτοποίηση της αιτίας της νεφρικής νόσου και στην εκτίμηση της σοβαρότητάς της. Επίσης, θα πρέπει να ταυτοποιεί τις συνέπειές της, να διερευνά για τυχόν συνυπάρχουσες καταστάσεις και να καθορίζει το ρυθμό απώλειας της νεφρικής λειτουργίας.
Ιστορικό
Η ΧΝΑ αφορά συνήθως μεσήλικες και υπερήλικες γάτες, 2,25,26 αν και οι νεαρές μπορούν να προσβληθούν επίσης. Αναφέρεται ότι ένα ποσοστό 10-15% από αυτές έχουν ηλικία μικρότερη των τριών ετών. 8 Η αξιολόγηση της νεφρικής λειτουργίας είναι επιβεβλημένη στις ηλικιωμένες γάτες, καθώς η ΧΝΝ προσβάλλει μέχρι το 31% ή 32% των γατών ηλικίας μεγαλύτερης των 10 ή 15 χρονών, αντίστοιχα. 2 Γενικά, η ΧΝΝ εμφανίζεται σε ποσοστό από 1,6% 27 έως 20% των γατών που εξετάζονται για διάφορους λόγους. 28
Δεν έχει αναφερθεί προδιάθεση ως προς το φύλο, αν και έχει βρεθεί μια μικρή αύξηση της συχνότητας του νοσήματος στα αρσενικά ζώα. 26 Πρόσφατα, οι White και συν. 29 ανέφεραν ότι οι αρσενικές γάτες εκτίθενται στη ΧΝΝ σε ηλικία μικρότερη από ότι οι θηλυκές. Σε ότι αφορά τη ΧΝΝ η επίδραση των ορμονών του φύλου έχει διαπιστωθεί στους ανθρώπους και θα μπορούσε να αποτελέσει μία λογική εξήγηση. Αντίθετες παρατηρήσεις υφίστανται σε στειρωμένες γάτες που αποτελούν τον πληθυσμό αναφοράς ενός ιατρείου. 29 Οι γάτες των φυλών Maine coon, Αβησσυνίας, Siamése, Russian blue, Περσική, Angora και Burmese προσκομίζονται συχνότερα με ΧΝΝ σε σχέση με άλλες φυλές. 2 Ωστόσο, αυτό εξαρτάται από τον πληθυσμό που μελετάται, στην κλινική μας όπως πιθανόν και σε άλλες, 18 προσκομίζονται συνήθως γάτες της φυλής Siamése και σε μικρότερο ποσοστό της βραχύτριχης κοινής Ευρωπαϊκής φυλής (DSH). Οικογενής προδιάθεση σε νεφρική νόσο που καταλήγει σε ΧΝΑ διαπιστώνεται σε συγκεκριμένες φυλές, όπως η πολυκυστική νόσος των νεφρών στις Περσικές, και η αμυλοείδωση στις Αβησσυνίας και πιθανόν στις Ragdoll. 30
Συμπτώματα
Οι γάτες μπορεί να προσκομιστούν με διάφορα συμπτώματα των οποίων η σοβαρότητα φαίνεται να ποικίλλει ανάλογα με την παρουσία ή όχι ουραιμίας. Οι ιδιοκτήτες συνήθως αναζητούν κτηνιατρική βοήθεια όταν τα συμπτώματα είναι έντονα, κάτι που υποδηλώνει προχωρημένη νόσο. Ωστόσο, η γάτα μπορεί αρχικά να προσκομιστεί χωρίς κανένα σύμπτωμα ή να παρουσιάζει πολυουρία/ πολυδιψία που εμμένει για εβδομάδες ή μήνες (1 ου σταδίου ΧΝΑ). Η πολυουρία/πολυδιψία, που αποτελεί ένα μάλλον σταθερό εύρημα στους σκύλους με ΧΝΑ, σε μία μελέτη καταγράφηκε μόνο στο 40% των γατών με ΧΝΑ. 18 Πέραν αυτού, μειωμένη όρεξη, απώλεια βάρους και κακή όψη του τριχώματος μπορούν να διαπιστωθούν στο αρχικό στάδιο της νόσου, ενώ στα προχωρημένα στάδια, εμφανίζονται εντονότερα συμπτώματα (ουραιμία) που περιλαμβάνουν σποραδικούς (τουλάχιστον στην αρχή) εμέτους, διάρροια και αλλοιώσεις στους οφθαλμούς. 8 Ο έμετος δεν αποτελεί κοινό σύμπτωμα στις γάτες με ΧΝΑ, πιθανώς λόγω της χαμηλής συχνότητας εμφάνισης γαστρίτιδας. 18 Αν και σπάνια, η τύφλωση μπορεί να είναι το μόνο σύμπτωμα που παρατηρούν οι ιδιοκτήτες. 6,31
Κλινική εξέταση
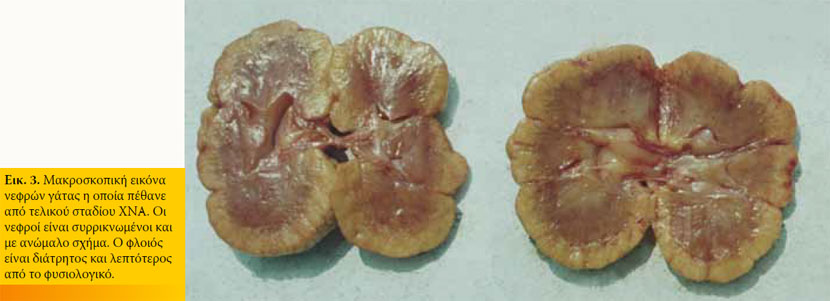
Γενικά, τα ευρήματα της κλινικής εξέτασης σε γάτες με ΧΝΝ είναι μη ειδικά. Ανάλογα με το στάδιο της νόσου η γάτα μπορεί να προσκομιστεί με αφυδάτωση και απώλεια βάρους, κακή όψη του τριχώματος, κατάπτωση, ωχρότητα των βλεννογόνων, έλκη στη στοματική κοιλότητα, δύσοσμη αναπνοή, σιαλόρροια, ασθενή σφυγμό, δύσπνοια και υποθερμία. 6,8 Κατά την ψηλάφηση της κοιλιακής κοιλότητας μπορεί να διαπιστωθούν ανώμαλοι, ανώδυνοι και μικροί σε μέγεθος νεφροί, που κατά την εμπειρία των συγγραφέων αποτελούν ένα μάλλον ευκαιριακό εύρημα σε γάτες με ΧΝΝ (Εικ.3). Επίσης μπορεί να υφίσταται νεφρομεγαλία, συνήθως όμως αναφέρονται νεφροί φυσιολογικού μεγέθους. 18 Κατά την ακρόαση του θώρακα μπορεί να διαπιστωθεί αρρυθμία και καρδιακό φύσημα, καθώς και αυξημένης έντασης αναπνευστικοί ήχοι ή ρόγχοι. Στα ευρήματα στους οφθαλμούς περιλαμβάνονται το ύφαιμα ή το οίδημα, η αιμορραγία, η αποκόλληση, καθώς και η ελικοειδής πορεία των αγγείων του αμφιβληστροειδή. 31
Εργαστηριακή διερεύνηση
Η έγκαιρη αναγνώριση της ΧΝΝ στις γάτες είναι καίριας σημασίας. Η θεραπευτική παρέμβαση στα αρχικά της στάδια, μπορεί να καθυστερήσει ή να αποτρέψει την εξέλιξή της. 4,7 Η διαγνωστική προσέγγιση της νεφρικής νόσου βασίζεται κυρίως στα εργαστηριακά ευρήματα, καθώς το ιστορικό και τα συμπτώματα είναι συνήθως μη ειδικά. Βέβαια, η μακροχρόνια πολυουρία/πολυδιψία ή/και οι μικροί σε μέγεθος νεφροί (αμφοτερόπλευρα ή ετερόπλευρα) κατά την ψηλάφηση οδηγούν σε σοβαρή υποψία ΧΝΑ. 6
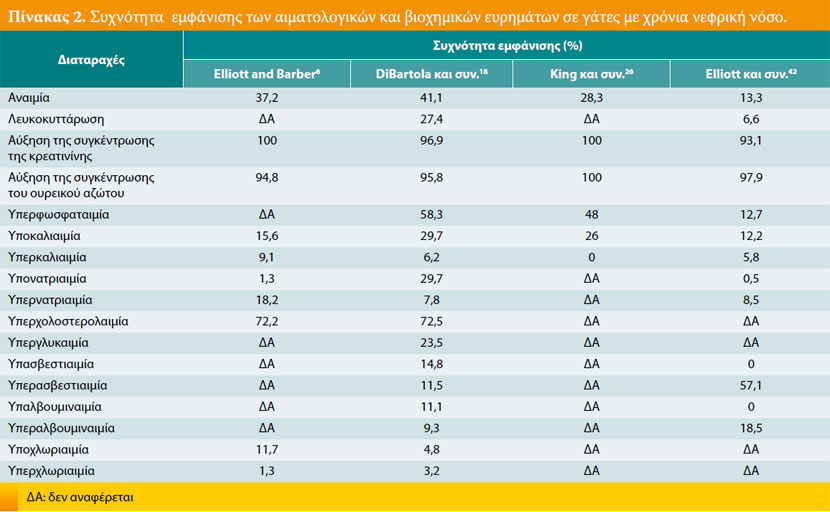
Τα διάφορα αιματολογικά και βιοχημικά ευρήματα που αναφέρονται σε γάτες με ΧΝΑ παραθέτονται στον Πίνακα 2. Οι γάτες με ΧΝΑ ενδέχεται να παρουσιαστούν με ήπιου έως μέτριου βαθμού ορθόχρωμη και ορθοκυτταρική μη αναγεννητική αναιμία. 2 Η λευκοκυττάρωση είναι συνήθως δευτερογενής της υποκείμενης αιτίας. Η αζωθαιμία αποτελεί την κύρια βιοχημική διαταραχή, η οποία χαρακτηρίζεται από αυξημένη συγκέντρωση του αζώτου ουρίας και της κρεατινίνης στον ορό του αίματος. Παρόλα αυτά, έχει αναφερθεί ότι ένα ποσοστό 60% των γατών με ΧΝΑ έχει αυξημένη συγκέντρωση φωσφόρου και το 20-30% αυτών έχουν μειωμένη συγκέντρωση καλίου, 31 ενώ το κάλιο αυξάνεται στο 15% των περιστατικών. 6 Η συγκέντρωση του ασβεστίου είναι αυξημένη, μειωμένη ή φυσιολογική. 8 Οι συγκεντρώσεις του μαγνησίου και του νατρίου μειώνονται 6,25 ή είναι συνήθως φυσιολογικές. Η συγκέντρωση του χλωρίου μειώνεται κυρίως όταν συνυπάρχει μεταβολική οξέωση, εύρημα που συχνά συνοδεύει το προχωρημένο στάδιο της νόσου (4ου σταδίου ΧΝΝ). 24 Φαίνεται ότι η οξέωση παρατηρείται πιο συχνά σε γάτες με ουραιμική κρίση, 6 αν και ο μηχανισμός για τη διατήρηση του pH σε φυσιολογικά επίπεδα στο 1ο και 2ο στάδιο της ΧΝΝ ακόμα ερευνάται.24 Η οξέωση θα πρέπει να επιβεβαιώνεται από την ανάλυση των αερίων του αρτηριακού αίματος και η συγκέντρωση των διττανθρακικών θα πρέπει να είναι μικρότερη από 17 mEq/L, ενώ αυτή του ολικού CO2 μικρότερη από 15 mmol/L. 2 Υπερχολοστερολαιμία έχει βρεθεί επίσης σε γάτες με ΧΝΑ, η οποία δεν ήταν δευτερογενής της σπειραματονεφρίτιδας. 6,18 Η ενδεχόμενη αύξηση της δραστηριότητας της λιπάσης και της αμυλάσης στον ορό του αίματος μπορεί να οφείλεται στη μειωμένη απομάκρυνσή τους από τους νεφρούς. 14 Σύμφωνα με την εμπειρία των συγγραφέων οι σταθερές βιοχημικές διαταραχές στις γάτες με ΧΝΑ, όταν αυτές υφίστανται, είναι η αζωθαιμία και η υπερφωσφαταιμία.
Η ανάλυση του ούρου είναι απαραίτητη για την αξιολόγηση του ουροποιητικού συστήματος. Στη ΧΝΝ, η μειωμένη ικανότητα των νεφρών να συμπυκνώνουν το ούρο έχει ως αποτέλεσμα τη μείωση του ειδικού βάρους του ούρου (ΕΒΟ) το οποίο είναι συνήθως μικρότερο του 1035 και κυμαίνεται μεταξύ 1008 και 1015.2,4 Ορισμένες γάτες πιθανώς να διατηρούν την ικανότητα συμπύκνωσης του ούρου, έτσι, το εύρημα αυτό δεν θα πρέπει να παραπλανά τον κλινικό στην απόφασή του για το εάν πρόκειται για προνεφρική ή μετανεφρική αζωθαιμία. Η πρωτεϊνουρία μπορεί να εμφανίζεται ακόμη και σε απουσία σπειραματοπάθειας, και έχει συνδεθεί με μικρότερο χρόνο επιβίωσης26 ή με αρτηριακή υπέρταση.32 Οι Minkus και συν.12 επιμένουν ότι όταν διαπιστωθεί πρωτεϊνουρία σε γάτες με ΧΝΑ, λόγω χρόνιας διαμεσοσωληναριακής νεφρίτιδας, τότε πάντα συνυπάρχει σπειραματονεφρίτιδα. Η πρωτεϊνουρία μπορεί να εκτιμηθεί χονδροειδώς μέσω της δοκιμής καθίζησης με σουλφοσαλικυλικό οξύ, ωστόσο αντικειμενικός δείκτης είναι ο λόγος πρωτεϊνών προς κρεατινίνη στο ούρο, ο οποίος θα πρέπει να είναι πάνω από 0,4.3,4,22,23 Στην κλινική μας, η πρωτεϊνουρία αποτελεί ένα μάλλον σποραδικό εύρημα στις γάτες με ΧΝΑ. Η μικροπρωτεϊνουρία είναι ένα σημαντικό διαγνωστικό εργαλείο, το οποίο μπορεί να συμβάλει στην ανεύρεση του υποκείμενου αιτιολογικού παράγοντα.4,7,22 Η ΧΝΑ δε συνοδεύεται συνήθως από ενεργό ίζημα ούρου,4 εκτός και αν αυτό συνδέεται με τον αιτιολογικό παράγοντα (π.χ. πυελονεφρίτιδα).14 Αν και δεν υπάρχει κάποιος πρακτικός βιολογικός δείκτης που να μπορεί αξιόπιστα να ανιχνεύσει τη ΧΝΝ σε πρώιμο στάδιο, ο καθορισμός του λόγου πρωτεϊνών προς κρεατινίνη στο ούρο σε συνδυασμό με τη συγκέντρωση της κρεατινίνης στον ορό του αίματος έχουν προταθεί ως πιθανοί προγνωστικοί δείκτες ανάπτυξης αζωθαιμίας στις ηλικιωμένες γάτες.33
Σε περιπτώσεις δευτερογενούς ή πρωτογενούς βακτηριδιακής λοίμωξης της κατώτερης ουροφόρου οδού, θα πρέπει να διενεργείται καλλιέργεια ούρου. Η πυελονεφρίτιδα μπορεί να οδηγήσει σε ΧΝΑ.7 Οι ηλικιωμένες γάτες είναι επιρρεπείς στις λοιμώξεις του ουροποιητικού συστήματος εξαιτίας του διαταραγμένου ανοσοποιητικού τους συστήματος ή της ΧΝΝ που περιορίζει την τοπική ανοσία. Τελικά, το αραιωμένο ούρο χάνει τις αντιβακτηριδιακές του ιδιότητες.7,34 Το χαμηλό ειδικό βάρος του ούρου μπορεί να οδηγήσει σε αρνητικά αποτελέσματα κατά την ανάλυση του. Σε μία μελέτη, οι 17 από τις 77 γάτες με ΧΝΝ είχαν λοίμωξη της ουροφόρου οδού, αν και μόνο 4 από αυτές παρουσίαζαν συμπτώματα νόσου της κατώτερης ουροφόρου οδού και ένας μεγάλος αριθμός δεν είχε λευκά αιμοσφαίρια ή βακτηρίδια στο ίζημα του ούρου.34
Οι ακτινογραφίες μπορούν να συμβάλουν στην αξιολόγηση της ακεραιότητας των νεφρών και στην αιτιολογική διάγνωση. Οι ακτινογραφίες και ο υπερηχοτομογράφημα του ανώτερου και κατώτερου ουροποιητικού συστήματος ενδέχεται να αποκλείσουν άλλες πιθανές αιτίες των συμπτωμάτων της γάτας. Πέραν τούτου, είναι δυνατό να ανιχνευθούν ουρόλιθοι στο ανώτερο ουροποιητικό συστήμα, υδρονέφρωση, πολυκυστικοί νεφροί ή νεόπλασμα των νεφρών. Η αξονική τομογραφία και η απεκκριτική ουρογραφία μπορούν να χρησιμοποιηθούν για την αξιολόγηση του ΡΣΔ και για την επιβεβαίωση της αιτιολογικής διάγνωσης.12,16
Η αξιολόγηση του ΡΣΔ θα πρέπει να χρησιμοποιείται για τη διάγνωση της ΧΝΝ, τουλάχιστον στα αρχικά στάδια (1ο ή 2ο στάδιο), όπου η συγκεντρώση της κρεατινίνης στον ορό του αίματος ενδέχεται να μην είναι ενδεικτική. Δυστυχώς, ο ΡΣΔ δεν μας παρέχει πληροφορίες για το ποσοστό του νεφρικού ιστού που έχει προσβληθεί. Μία χονδροειδής εκτίμηση του ΡΣΔ μπορεί να γίνει σε επίπεδο ρουτίνας με τον απλό προσδιορισμό της ενδογενούς κρεατινίνης στον ορό του αίματος. Είναι αξιοσημείωτο ότι τιμή κρεατινίνης στον ορό του αίματος που βρίσκεται κοντά στην ανώτερη τιμή του ορίου αναφοράς μπορεί να αντανακλά μειωμένο ΡΣΔ. Η εξωγενής χορήγηση διάφορων ουσιών που αποβάλλονται κυρίως από τους νεφρούς, όπως η κρεατινίνη, η ινουλίνη ή η ιοχεξόλη αποτελεί καλύτερο δείκτη του ΡΣΔ. Το σημείο-κλειδί της δοκιμής αυτής είναι ότι μετά από τη χορήγηση της ουσίας, το επίπεδο της συγκέντρωσής της στο πλάσμα του αίματος ή στο ούρο αντανακλά το ρυθμό της αποβολής της από τους νεφρούς.4,20,35 Πιθανώς, η δοκιμή αυτή μπορεί να αποδειχθεί χρήσιμη και στην εκτίμηση του ΡΣΔ σε περιστατικά με προχωρημένη νόσο (3ου ή 4ου σταδίου) όπου η απώλεια της μυϊκής μάζας θα μπορούσε να συμβάλει στη μείωση της συγκέντρωσης της κρεατινίνης στον ορό του αίματος.
Συστηματική υπέρταση έχει παρατηρηθεί σε ένα 20% των γατών με ΧΝΝ,31 αν και έχουν επίσης αναφερθεί ποσοστά της τάξης 60-65%.36,37 Το μεγάλο εύρος πιθανώς να αντανακλά την προέλευση των μελετών, λαμβάνοντας υπόψη την απόκλιση αυτών που προέρχονται από κλινικές πρώτης και δεύτερης γνώμης. 31 Παραμένει ενδιαφέρον το γεγονός ότι το ποσοστό εμφάνισης αρτηριακής υπέρτασης, δευτερογενώς της ΧΝΝ, στις γάτες που εξετάσαμε ήταν μικρό. Ωστόσο, ο υπολογισμός της πίεσης του αίματος είναι καθοριστικός εξαιτίας των συστηματικών, καθώς και των νεφρικών συνεπειών της υπέρτασης.38 Επιπλέον, η αρτηριακή υπέρταση απαιτεί ειδική θεραπευτική διαχείριση και καθορίζει την πρόγνωση, εάν και, εφόσον αντιμετωπιστεί, δε φαίνεται να επηρεάζει το χρόνο επιβίωσης.32 Όπως έχει αναφερθεί, θα πρέπει ακόμα να καθορίζονται και οι αλλοιώσεις στους οφθαλμούς λόγω της υπέρτασης.31,38
H χειρουργική ή μέσω υπερηχοτομογραφικής καθοδήγησης βιοψία των νεφρών και η επακόλουθη ιστοπαθολογική εξέταση μπορούν να καταλήξουν σε αιτιολογική διάγνωση.7 Αναφέρεται ότι στις περισσότερες γάτες (70,4%) ανιχνεύθηκε ιστολογικά χρόνια διαμεσοσωληναριακή νεφρίτιδα.12 Αν και η ιστοπαθολογική εξέταση είναι μία μάλλον μη ευαίσθητη μέθοδος για την αιτιολογική διάγνωση της ΧΝΝ, αποτελεί τον ακρογωνιαίο λίθο για τη διάγνωση της νεφρικής νόσου πριν από την εγκατάσταση της νεφρικής δυσλειτουργίας.20,25 Γενικά, αν και η βιοψία των νεφρών αποτελεί μία σχετικά εύκολη διαδικασία στη γάτα, στην πλειονότητα των περιστατικών ο κίνδυνος του χειρουργείου δεν εξισορροπείται από τα πιθανά οφέλη της.
Οι γάτες θα πρέπει επίσης να εξετάζονται για τον ιό της επίκτητης ανοσοανεπάρκειας (FIV), τον ιό της ιογενούς λευχαιμίας (FeLV) και τον ιό της λοιμώδους περιτονίτιδας (FIP), καθώς η ΧΝΝ και η πρόγνωσή της θα μπορούσε να σχετίζεται με αυτούς.14 Πρόσφατα αναφέρθηκε ότι γάτες με ΧΝΝ ηλικίας μικρότερης των 11 ετών ήταν πιθανότερο να βρεθούν θετικές στον ιό της επίκτητης ανοσοανεπάρκειας από ότι γάτες χωρίς ΧΝΝ.39 Διαφοροποίηση μεταξύ οξείας και χρόνιας νόσου θα πρέπει να γίνεται όταν διαπιστώνεται ουραιμική κρίση και θα πρέπει να βασίζεται στη μακροχρόνια πολυουρία/πολυδιψία, τους μικρούς σε μέγεθος και ανώμαλους κατά την ψηλάφηση νεφρούς και τη μη αναγεννητική αναιμία. Χρήσιμο σημείο διαφοροποίησης αποτελεί ότι η οξεία νεφρική ανεπάρκεια χαρακτηρίζεται από αρκετά έντονα συμπτώματα για σχετικά μικρό χρονικό διάστημα.40
Θα πρέπει να εκτιμώνται η καρδιακή λειτουργία, η λειτουργία του θυρεοειδή, ο υποφλοιοεπινεφριδισμός και η ύπαρξη σακχαρώδους διαβήτη ώστε να καθοριστούν οι προνεφρικές αιτίες αζωθαιμίας ή οι πρωτογενείς αιτίες της ΧΝΝ. Πρέπει να σημειωθεί ότι η δυνητική συνύπαρξη της ΧΝΝ με τον υπερθυρεοειδισμό σε ηλικιωμένες γάτες ενδέχεται να αποκρύψει τη βαρύτητα της ΧΝΑ, καθώς η υπερθυρεοειδική κατάσταση του οργανισμού βελτιώνει την ροή του αίματος στους νεφρούς και το ΡΣΔ.40
> Περιγραφή περιστατικού
Ο Λεοσθένης, ένας τεσσάρων ετών γάτος, Περσικής φυλής, αρσενικός, στειρωμένος, προσκομίστηκε με ιστορικό μειωμένης όρεξης, κατάπτωσης και σποραδικών επεισοδίων εμέτου. Κατά τη διάρκεια των τελευταίων 20 ημερών παρουσίασε πέντε επεισόδια εμέτων, που αποτελούνταν από γαστρικά υγρά. Ο ιδιοκτήτης του δεν είχε παρατηρήσει άλλα συμπτώματα, όπως πολυουρία/πολυδιψία.
Ιστορικό Ο Λεοσθένης ήταν υγιής καθόλη τη διάρκεια της ζωής του. Ζούσε μέσα στο σπίτι, εμβολιαζόταν και αποπαρασιτωνόταν τακτικά και διατρεφόταν με βιομηχανοποιημένη τροφή συντήρησης. Περίπου τρεις εβδομάδες νωρίτερα, υποβλήθηκε σε ρουτίνας αποτρύγωση των δοντιών με υπερήχους από τον παραπέμποντα κτηνίατρο. Η κλινική, η αιματολογική και η βιοχημική εξέταση που προηγήθηκαν της διαδικασίας δεν έδειξαν κάτι το αξιοσημείωτο και η ανάνηψη από την αναισθησία ήταν φυσιολογική. Ωστόσο, ο Λεοσθένης εμφάνισε συμπτώματα μειωμένης όρεξης και κατάπτωσης, τα οποία αποδόθηκαν στη δυσάρεστη αίσθηση από τον ερεθισμό των ούλων. Όταν παρουσιάστηκε έμετος, τέθηκε υποψία γαστροοισοφαγικής παλινδρόμησης ή/και οξείας γαστρίτιδας και συνταγογραφήθηκαν ρανιτιδίνη, μετοκλοπραμίδη και σουκραλφάτη. Ενώ η κατάσταση του γάτου παρέμενε αμετάβλητη, περίπου 15 ημέρες αργότερα η γενική εξέταση του αίματος και ο έλεγχος των βιοχημικών παραμέτρων στον ορό του αίματος έδειξαν σοβαρή αζωθαιμία.
Κλινική και εργαστηριακή εκτίμηση Ο Λέοσθένης κατά την προσκόμιση ήταν μέτρια αφυδατωμένος και εμφάνιζε κατάπτωση. Ο αιματοκρίτης ήταν στα κατώτερα φυσιολογικά όρια (25,3%: τιμές αναφοράς: 24-45%), ενώ το άζωτο ουρίας (160 mg/dl: τιμές αναφοράς: 9-32 mg/dl), η κρεατινίνη (4,1 mg/dl: τιμές αναφοράς: 0,7-1,6 mg/dl) και ο φωσφόρος (8,9 mg/dl: τιμές αναφοράς: 3,5- 6,7 mg/dl) ήταν σημαντικά αυξημένα. Το κάλιο (2,2 mEq/L: τιμές αναφοράς: 3,4-5,4 mEq/L) ήταν μειωμένο, το ΕΒΟ ήταν 1017, ενώ στην εξέταση του ιζήματος του ούρου δεν υπήρχαν παθολογικά ευρήματα.
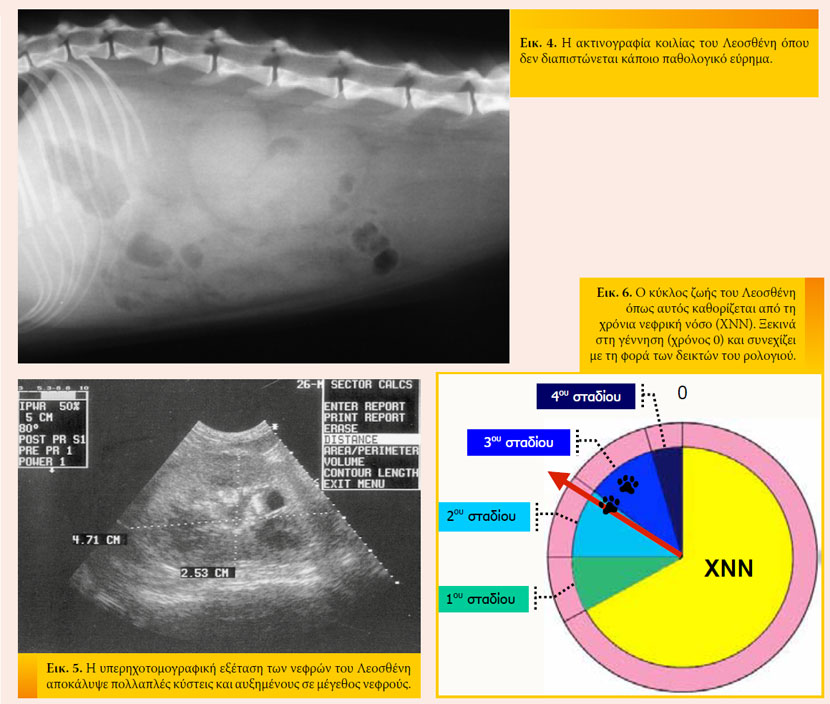
Αρχικά μέτρα και περαιτέρω διαγνωστική προσέγγιση Αρχικά χορηγήθηκαν ενδοφλέβια υγρά ενισχυμένα με κάλιο και ρανιτιδίνη. Η ακτινολογική διερεύνηση της κοιλιακής κοιλότητας έδειξε ότι το μέγεθος των νεφρών (ειδικά του δεξιού) ήταν στα ανώτερα φυσιολογικά όρια (Εικ. 4), ενώ στο υπερηχοτομογράφημα διαπιστώθηκαν πολλαπλές κύστεις και διευρυμένο το μέγεθος και των δύο νεφρών (Εικ. 5). Ο λόγος πρωτεϊνών/κρεατινίνης στο ούρο ήταν φυσιολογικός και η καλλιέργεια αρνητική. Ακόμα, η πίεση του αρτηριακού αίματος ήταν μέσα στα φυσιολογικά όρια.
Διάγνωση Η αιτιολογική διάγνωση ήταν η πολυκυστική νόσος των νεφρών των Περσικών γατών. Η αναισθησία ενδέχεται να προκάλεσε την κλινική εκδήλωση της ΧΝΝ.
Θεραπεία και έκβαση Στον Λεοσθένη δόθηκε εξιτήριο την 6η ημέρα της νοσηλείας του. Ήταν χαρούμενος, ενεργητικός, και έτρωγε ικανοποιητικά, αλλά ήταν ήπια αζωθαιμικός, υπερφωσφαταιμικός, ενώ το κάλιο βρισκόταν στα φυσιολογικά όρια. Για το σπίτι συνταγογραφήθηκαν ειδική δίαιτα για νεφροπαθείς γάτες, ρανιτιδίνη, δεσμευτής φωσφόρου και αναστολέας του μετατρεπτικού ενζύμου της αγγειοτενσίνης Ι. Διαδοχικοί προσδιορισμοί των βιοχημικών παραμέτρων στον ορό του αίματος έδειξαν σταθεροποίηση της κατάστασης του Λεοσθένη ο οποίος βρισκόταν πλέον στο 2ο στάδιο της ΧΝΝ, στο οποίο παραμένει μέχρι και σήμερα, ένα χρόνο αργότερα (Εικ. 6).
Τι υποδηλώνει το περιστατικό αυτό; Είναι γνωστό ότι υπάρχει οικογενής προδιάθεση των Περσικών γατών για την ανάπτυξη πολυκυστικής νόσου των νεφρών. Οι περισσότερες από τις γάτες αυτές εκδηλώνουν ΧΝΑ περίπου στην ηλικία των 7 ετών, αν και μερικές μπορεί να παραμείνουν κλινικά υγιείς για το μεγαλύτερο χρονικό διάστημα της ζωής τους ή να παρατηρηθεί ύφεση της νόσου.45 Συνεπώς, θα πρέπει να γίνεται προσεκτικός χειρισμός των ευπαθών γατών ώστε να προστατεύεται η νεφρική λειτουργία και η ακεραιότητα των νεφρών όταν επιχειρούνται επεμβατικές διαδικασίες. Η έγκαιρη αναγνώριση της νόσου είναι καίριας σημασίας. Η υπερηχοτομογραφική εξέταση προτείνεται ήδη από την ηλικία των 10 μηνών.45 Ο γονιδιακός έλεγχος, εφόσον είναι διαθέσιμος, αποτελεί μία αξιόπιστη διαγνωστική μέθοδο, χωρίς ωστόσο να καθορίζει τη σοβαρότητα της νεφρικής νόσου που δυνητικά θα εμφανιστεί.
> Συνέπειες της χρόνιας νεφρικής ανεπάρκειας
Στις γάτες με ΧΝΑ, ουραιμικές τοξίνες συσσωρεύονται στα σωματικά υγρά λόγω της απορρύθμισης της ικανότητας των νεφρών να απεκκρίνουν τα άχρηστα μεταβολικά προϊόντα. Αυτά τα οργανικά παράγωγα είναι υπεύθυνα για τις ποικίλες και πολυσυστηματικές συνέπειες ή επιπλοκές της νόσου. Επιπλέον, οι επιπλοκές της ΧΝΑ είναι αποτέλεσμα ορμονικών διαταραχών και της ανικανότητας των νεφρών να ρυθμίσουν τα σωματικά υγρά, καθώς και την οξεοβασική ισορροπία και την ηλεκτρολυτική ομοιοστασία.5
1. Πολυουρία και πολυδιψία
Η πολυουρία προκαλείται από μείωση της ικανότητας των νεφρών να συμπυκνώνουν το ούρο, η οποία είναι αποτέλεσμα της μειωμένης ανταπόκρισης των νεφρών στη δράση της αντιδιουρητικής ορμόνης, της διαταραχής της αρχιτεκτονικής δομής της μυελώδους μοίρας και της διούρησης του διηθήματος.40 Αντισταθμιστής της πολυουρίας είναι η πολυδιψία, η οποία φαίνεται να αναγνωρίζεται πιο εύκολα από τους ιδιοκτήτες των γατών.
2. Αρτηριακή υπέρταση
Όταν είναι παρούσες τόσο η αρτηριακή υπέρταση όσο και η ΧΝΝ, ο καθορισμός της σχέσης αιτίου και αιτιατού είναι δύσκολος.38 Η πρωτογενής αρτηριακή υπέρταση είναι πολύ κοινή στον άνθρωπο, ενώ η δευτερογενής αναφέρεται μέχρι και στο 66% των γατών με ΧΝΝ. Παρόλο που οι χαρακτηριστικές ιστοπαθολογικές αλλοιώσεις της υπέρτασης έχουν βρεθεί σε νεφρούς σκύλων και γατών με ΧΝΑ, η υπερτασική νεφροπάθεια που συναντάται στους ανθρώπους δεν φαίνεται να υφίσταται στα μικρά ζώα. Οι αλλοιώσεις αυτές πιστεύεται ότι είναι αποτέλεσμα της υπέρτασης που αναπτύσεται δευτερογενώς σε ΧΝΝ.2 Γενικά, η αρτηριακή πίεση φαίνεται να ρυθμίζεται από αδρενεργικά, νεφρικά, ενδοκρινικά και αγγειακά συστήματα και σχετίζεται με την καρδιακή παροχή και την περιφερική αντίσταση των αγγείων. Σε ζώα με ΧΝΑ, η απορρύθμιση της ομοιοστασίας των υγρών εξαιτίας του μειωμένου ΡΣΔ και της μειωμένης απέκκρισης του νατρίου, η αύξηση της καρδιακής παροχής, η διαταραχή της αντίστασης του τοιχώματος των αγγείων, η διαταραχή του συστήματος ρενίνης-αγγειοτασίνης-αλδοστερόνης καθώς και του συστήματος καλλικρεΐνης-κινίνης-προσταγλανδίνης και οι επιπτώσεις που σχετίζονται με τον υπερπαραθυρεοειδισμό έχουν ενοχοποιηθεί για την ανάπτυξη της υπέρτασης.17,38 Θα πρέπει να σημειωθεί ότι ο υπεραλδοστερονισμός οδήγησε σε υπέρταση σε ορισμένες γάτες με ΧΝΑ.41
3. Νεφρογενής δευτερογενής υπερπαραθυρεοειδισμός
Ο νεφρογενής δευτερογενής υπερπαραθυρεοειδισμός (ΝΔΥ) αποτελεί μία από τις πιο συχνές και σημαντικές επιπτώσεις της ΧΝΑ.42 Χαρακτηρίζεται από αύξηση της δραστηριότητας της παραθορμόνης στον ορό του αίματος και έχει παρατηρηθεί στο 80% περίπου των γατών με ΧΝΝ.40 Η αύξηση της συγκέντρωσης της παραθορμόνης είναι αποτέλεσμα της μειωμένης παραγωγής της καλσιτριόλης από τα κύτταρα των νεφρικών σωληναρίων και της κατακράτησης του φωσφόρου από τους νεφρούς.23 Η κατακράτηση του φωσφόρου οδηγεί σε υπερφωσφαταιμία, η οποία με τη σειρά της αναστέλλει τη μετατροπή της 25- υδροξυχολοκαλσιφερόλης στην πιο δραστική μορφή της βιταμίνης D, την καλσιτριόλη, από την 1α- υδροξυλάση. Η μειωμένη συγκέντρωση της καλσιτριόλης και συνεπακόλουθα του ασβεστίου στον ορό του αίματος, διεγείρει την παραγωγή της παραθορμόνης από τους παραθυρεοειδείς αδένες.2 Η παραθορμόνη θεωρείται ως μία από τις κύριες ουραιμικές τοξίνες,5 αν και σπάνια στις γάτες παρατηρούνται συμπτώματα του ΝΔΥ. Όταν αυξάνεται η συγκέντρωση της παραθορμόνης στον ορό του αίματος, προκαλείται κινητοποίηση του ασβεστίου από τον σκελετό, απασβέστωση των οστών (νεφρική οστεοδυστροφία) και στη συνέχεια επασβέστωση των μαλακών ιστών,23,42 καθώς και δυσλειτουργία διαφόρων οργάνων. Κυτταρική δυσλειτουργία παρατηρείται όταν τα επίπεδα του βασικού κυτταρικού ασβεστίου είναι σταθερά αυξημένα. Στον άνθρωπο, προσβάλλονται σε σοβαρότερο βαθμό τα οστά του κρανίου και της γνάθου και ενδέχεται να υπάρχει γενικευμένη αίσθηση άλγους.43 Τα αυξημένα επίπεδα της παραθορμόνης έχουν αντίστροφη επίδραση στον μεταβολισμό της γλυκόζης και των λιπιδίων, καθώς και στη λειτουργία του καρδιαγγειακού συστήματος και του ΚΝΣ. Πέραν αυτών, επιδεινώνουν την ανοσοανεπάρκεια και την αναιμία, οι οποίες ήδη αποτελούν επιπλοκές της ΧΝΑ της γάτας.44 Όπως έχει ήδη αναφερθεί, στα εργαστηριακά ευρήματα του ΝΔΥ περιλαμβάνονται η αυξημένη συγκέντρωση του φωσφόρου και της παραθορμόνης στον ορό του αίματος. Αυξημένος κίνδυνος για επασβέστωση υπάρχει όταν το γινόμενο των συγκεντρώσεων του φωσφόρου επί του ολικού ασβεστίου στον ορό του αίματος είναι μεγαλύτερο από 70.23 Πιο συχνά επηρεάζονται όργανα που εκκρίνουν πρωτόνια, όπως το στομάχι και οι νεφροί, μπορούν όμως να ασβεστοποιηθούν επίσης το μυοκάρδιο, οι πνεύμονες και το ήπαρ. Είναι αξιοσημείωτο ότι σε αρκετές γάτες με ΧΝΑ, παρατηρήθηκε υπερπαραθορμοναιμία παρά την απουσία υπερφωσφαταιμίας.40,43 Δευτερογενής παραθυρεοειδομεγαλία λόγω ΝΔΥ μπορεί να παρατηρηθεί ως μια ψηλαφήσιμη παρατραχειακή μάζα και δεν θα πρέπει να εκλαμβάνεται ως μάζα του θυρεοειδούς αδένα λόγω του υπερθυρεοειδισμού, που συχνά συνυπάρχει με τη ΧΝΝ.
4. Γαστρεντερικές διαταραχές
Γαστρεντερικές επιπλοκές, σε ποικίλους συνδυασμούς όπως ανορεξία, απώλεια βάρους και αιμορραγικός ή μη έμετος και διάρροια αποτελούν τα συμπτώματα που μπορεί να παρατηρηθούν ιδιαίτερα σε γάτες με προχωρημένου σταδίου ΧΝΑ (3ου ή 4ου σταδίου). Το στομάχι είναι το όργανο που προσβάλλεται συχνότερα, μπορεί όμως να παρατηρηθούν συμπτώματα και από τον υπόλοιπο γαστρεντερικό σωλήνα. Η ελκωτική γαστρίτιδα είναι αποτέλεσμα της υπεργαστριναιμίας, λόγω της μείωσης του ΡΣΔ. Τα αυξημένα επίπεδα γαστρίνης μπορούν να προκαλέσουν υπεροξέωση λόγω της αυξημένης παραγωγής ιόντων υδρογόνου από τα τοιχωματικά κύτταρα του γαστρικού βλεννογόνου. Ακόμη μερικοί επιπλέον παράγοντες που μπορεί να συμβάλουν σε ελκωτική γαστρίτιδα είναι το στρες του νοσήματος, η ισχαιμία του γαστρικού βλεννογόνου και η διαταραχή της παραγωγής της γαστρικής βλέννης που έχουν σαν αποτέλεσμα την εξασθένηση του γαστρικού βλεννογόνιου φραγμού. Τελικά, οι αυξημένες συγκεντρώσεις της αμμωνίας και της ουρίας οδηγούν σε ξηρότητα, υπεραιμία, διάβρωση και εξέλκωση του γαστρεντερικού βλεννογόνου και μπορούν να προκαλέσουν ελκωτική στοματίτιδα, οισοφαγίτιδα, γαστρίτιδα και εντεροκολίτιδα.23
5. Αναιμία
Οι γάτες με ΧΝΝ εμφανίζουν συνήθως μη αναγεννητική, ορθοκυτταρική και ορθόχρωμη αναιμία η οποία μπορεί να είναι πολυπαραγοντική.40 Η κυριότερη αιτία της αναιμίας είναι η ανεπάρκεια σε ερυθροποιητίνη λόγω της ανεπαρκούς ικανότητας των περισωληναριακών ινοβλαστών της φλοιώδους μοίρας των νεφρών ή/και των διάμεσων ινοβλαστών να τη συνθέσουν.6 Είναι αξιοσημείωτο ότι τα επίπεδα της ερυθροποιητίνης στο πλάσμα του αίματος αναιμικών γατών που πάσχουν από ΧΝΝ είναι χαμηλότερα από αυτά αναιμικών γατών που δεν πάσχουν από ΧΝΝ, ενώ είναι ανάλογα με αυτά υγιών γατών. Η χρόνια απώλεια αίματος από το γαστρεντερικό σωλήνα, ο υποσιτισμός, η υποπρωτεϊναιμία, η απώλεια βάρους, η ανεπάρκεια βιταμινών ή άλλων θρεπτικών στοιχείων, η μείωση της διάρκειας ζωής των ερυθροκυττάρων, οι ερυθροποιητικοί αποκλειστές στο ουραιμικό πλάσμα, η μυελοΐνωση, η αιμορραγική διάθεση λόγω δυσλειτουργίας των αιμοπεταλίων και οι επιδράσεις της χρόνιας νόσου αποτελούν επιπρόσθετους παράγοντες που συμβάλουν στην αναιμία που σχετίζεται με τη ΧΝΝ στις γάτες.2,40
6. Διαταραχές της οξεοβασικής ισσοροπίας και της συγκέντρωσης των ηλεκτρολυτών
Η υποκαλιαιμία είναι μία από τις πιο σημαντικές ηλεκτρολυτικές διαταραχές σε γάτες με ΧΝΑ.44 Είναι το αποτέλεσμα της μειωμένης πρόσληψης του καλίου, της μειωμένης επαναρρόφησής του, της απώλειάς του από τους νεφρούς, της διαταραχής της οξεοβασικής ισορροπίας και της μειωμένης συγκέντρωσης του μαγνησίου στον ορό του αίματος,25,31 και μπορεί να αναπτυχθεί αρκετά αργότερα από τη μείωση της περιεκτικότητας των μυών σε κάλιο. Η αποκατάσταση της νορμοκαλιαιμίας θεωρείται επιβεβλημένη, εξαιτίας της δυσλειτουργίας του ΡΣΔ που προκαλείται από την ελάττωση της συγκέντρωσης του καλίου. Όπως αναφέρθηκε προηγουμένως, η υπερφωσφαταιμία είναι η πιο συχνή ηλεκτρολυτική διαταραχή σε γάτες με αζωθαιμία λόγω ΧΝΑ και αφορά μέχρι και το 80% των περιστατικών.2 Με βάση την εμπειρία των συγγραφέων η κυρίαρχη ηλεκτρολυτική διαταραχή σε αζωθαιμικές γάτες λόγω ΧΝΝ είναι η υπερφωσφαταιμία.
 Η συντριπτική πλειονότητα των γατών με ΧΝΑ που συνοδεύεται από διαταραχή της οξεοβασικής ισσοροπίας εμφανίζουν μεταβολική οξέωση, η οποία οφείλεται στη μειωμένη επαναρρόφηση των διττανθρακικών, τη μειωμένη παραγωγή αμμωνίας από τους νεφρούς καθώς και στη μειωμένη απέκκριση από αυτούς των ιόντων υδρογόνου.2,44 Σε ένα μικρό αριθμό περιστατικών ενδέχεται να παρατηρηθεί μεταβολική αλκάλωση. Σε μία αναδρομική μελέτη που αφορούσε σε γάτες με ΧΝΑ, μεταβολική οξέωση διαπιστώθηκε στο 50% των γατών με νόσο τελικού σταδίου, στο 15% με μέτριου βαθμού νόσο και σπάνια σε περιστατικά 1ου ή 2ου σταδίου. Σε οξεία ουραιμική κρίση, η οξέωση είναι δυνατόν να προκαλέσει μείωση της ελαστικότητας των περιφερικών και των πνευμονικών αγγείων που θα μπορούσε να αυξήσει τον κίνδυνο ανάπτυξης πνευμονικού οιδήματος. Η μεταβολική οξέωση μεγάλης διάρκειας αυξάνει την αποδόμηση των πρωτεϊνών, επιδεινώνει τη νεφρικής αιτιολογίας οστεοδυστροφία και καταλήγει σε περαιτέρω νεφρική βλάβη.24
Η συντριπτική πλειονότητα των γατών με ΧΝΑ που συνοδεύεται από διαταραχή της οξεοβασικής ισσοροπίας εμφανίζουν μεταβολική οξέωση, η οποία οφείλεται στη μειωμένη επαναρρόφηση των διττανθρακικών, τη μειωμένη παραγωγή αμμωνίας από τους νεφρούς καθώς και στη μειωμένη απέκκριση από αυτούς των ιόντων υδρογόνου.2,44 Σε ένα μικρό αριθμό περιστατικών ενδέχεται να παρατηρηθεί μεταβολική αλκάλωση. Σε μία αναδρομική μελέτη που αφορούσε σε γάτες με ΧΝΑ, μεταβολική οξέωση διαπιστώθηκε στο 50% των γατών με νόσο τελικού σταδίου, στο 15% με μέτριου βαθμού νόσο και σπάνια σε περιστατικά 1ου ή 2ου σταδίου. Σε οξεία ουραιμική κρίση, η οξέωση είναι δυνατόν να προκαλέσει μείωση της ελαστικότητας των περιφερικών και των πνευμονικών αγγείων που θα μπορούσε να αυξήσει τον κίνδυνο ανάπτυξης πνευμονικού οιδήματος. Η μεταβολική οξέωση μεγάλης διάρκειας αυξάνει την αποδόμηση των πρωτεϊνών, επιδεινώνει τη νεφρικής αιτιολογίας οστεοδυστροφία και καταλήγει σε περαιτέρω νεφρική βλάβη.24
> Συμπέρασμα
Η ΧΝΝ αποτελεί μία πολύ συχνή παθολογική κατάσταση που απαντάται στις ηλικιωμένες γάτες. Στα περισσότερα περιστατικά η αιτιολογία δεν αποσαφηνίζεται. Η διαγνωστική προσέγγιση αφορά στην αξιολόγηση της αιτίας της ΧΝΝ, τη σοβαρότητα της (σταδιοποίηση), καθώς και τις επιδράσεις της στους νεφρούς και σε άλλα όργανα ή συστήματα του οργανισμού. Επιπλέον, η διάγνωση έχει ως σκοπό την υιοθέτηση των κατάλληλων μέτρων και τον καθορισμό της πρόγνωσης της νόσου.
> ΒΙΒΛΙΟΓΡΑΦΙΑ
1. Lawler DF, Evans RH, Chase K, Ellersieck M, Li Q, Larson BT, Satyarai E, Heininqer K. The aging feline kidney: a model mortality antagonist? J Feline Med Surg 2006, 8: 363-371.
2. Ross SJ, Polzin DJ, Osborne CA. Clinical progression of early chronic renal failure and implications for management. In: Consultations in Feline Internal Medicine. August JR (ed). Vol 5. Elsevier Saunders: St Louis, 2006, pp. 389-398.
3. White JD, Malik R, Norris JM. Feline chronic kidney disease: can we move from treatment to prevention? Vet J 2011, doi: 10.1016/j.tvjl.2010.12.011.
4. Lees GE. Early diagnosis of renal disease and renal failure. Vet Clin Small Anim Pract 2004, 34: 867-885.
5. Glassock RJ. Uremic toxins: what are they? An integrated overview of pathobiology and classification. J Ren Nutr 2008, 18: 2-6.
6. Elliott J, Barber PJ. Feline chronic renal failure: clinical findings in 80 cases diagnosed between 1992 and 1995. J Small Anim Pract 1998, 39: 78-85.
7. Grauer GF. Early detection of renal damage and disease in dogs and cats. Vet Clin Small Anim Pract 2005, 35: 581-596.
8. Sturgess K. Renal disease. In: Notes in Feline Internal Medicine. Blackwell Science Ltd: Oxford, 2003, pp. 147-165.
9. Cannon MJ, MacKay AD, Barr FJ, Rudorf H, Bradley KJ, Gruffydd-Jones TJ. Prevalence of polycystic kidney disease in Persian cats in the United Kingdom. Vet Rec 2001, 149: 409-411.
10. Barthez PY, Rivier P, Begon D. Prevalence of polycystic kidney disease in Persian and Persian related cats in France. J Feline Med Surg 2003, 5: 345-347.
11. Ross SJ, Osborne CA, Lekcharoensuk C, Koehler LA, Polzin DJ. A case-control study of the effects of nephrolithiasis in cats with chronic kidney disease. J Am Vet Med Assoc 2007, 230: 1854-1859.
12. Minkus G, Reusch C, Hörauf A, Breuer W, Darbès J, Kraft W, Hermanns W. Evaluation of renal biopsies in cats and dogs-histopathology in comparison with clinical data. J Small Anim Pract 1994, 35: 465-472.
13. Lappin MR, Jensen WA, Jensen TD, Basaraba RJ, Brown CA, Radecki SV, Hawley JR. Investigation of the induction of antibodies against Crandell-Rees feline kidney cell lysates and feline renal cell lysates after parenteral administration of vaccines against feline viral rhinotracheitis, calicivirus and panleukopenia in cats. Am J Vet Res 2005, 66: 506-511.
14. Polzin DJ, Osborne CA, Ross S. Chronic kidney disease. In: Textbook of Veterinary Medicine. Diseases of the Dog and Cat. Ettinger SJ, Feldman EC (eds). 6th edn. Vol 2. Elsevier Saunders: St Louis, 2005, pp. 1756-1785.
15. German AC, Harbour DA, Helps CR, Gruffydd-Jones TJ. Is feline foamy virus really apathogenic? Vet Immunol Immunopathol 2008, 123: 114-118.
16. Kyles AE, Hardie EM, Wooden BG, Adin CA, Stone EA, Gregory CR, Mathews KG, Cowgill LD, Vaden S, Nyland TG, Ling GV. Clinical, clinicopathologic, radiographic, and ultrasonographic abnormalities in cats with ureteral calculi: 163 cases (1984-2002). J Am Vet Med Assoc 2005, 226: 932-936.
17. Watanabe T, Mishina M. Effects of benazepril hydrochloride in cats with experimentally induced or spontaneously occurring chronic renal failure. J Vet Med Sci 2007, 69: 1015-1023.
18. DiBartola SP, Rutgers HC, Zack PM, Tarr MJ. Clinicopathologic findings associated with chronic renal disease in cats: 74 cases (1973-1984). J Am Vet Med Assoc 1987, 190: 1196-1202.
19. Ross SJ, Osborne CA, Kirk CA, Lowry SR, Koehler LA, Polzin DJ. Clinical evaluation of dietary modification for treatment of spontaneous chronic kidney disease in cats. J Am Vet Med Assoc 2006, 229: 949-957.
20. Finco DR, Brown SA, Brown CA, Crowell WA, Cooper TA, Barsanti JA. Progression of chronic renal disease in the dog. J Vet Intern Med 1999, 13: 516-528.
21. Brown SA, Brown CA, Jacobs G, Stiles J, Hendi RS, Wilson S. Effects of the angiotensin converting enzyme inhibitor benazepril in cats with induced renal insufficiency. Am J Vet Res 2001, 62: 375-383.
22. Syme H. Proteinuria in cats. Prognostic marker or mediator? J Feline Med Surg 2009, 11: 211-218.
23. Plotnick A. Feline chronic renal failure: long-term medical management. Compend Contin Educ Pract Vet 2007, 29: 342-351.
24. Elliott J, Syme HM, Markwell PJ. Acid-base balance of cats with chronic renal failure: effect of deterioration in renal function. J Small Anim Pract 2003, 44: 261-268.
25. Adams LG, Polzin DJ, Osborne CA, O’Brien TD. Effects of dietary protein and calorie restriction in clinically normal cats and in cats with surgically chronic renal failure. Am J Vet Res 1993, 54: 1653-1662.
26. King JN, Tasker S, Gunn-Moore DA, Strehlau G, BENRIC (Benazepril in renal insufficiency in cats) Study Group. Prognostic factors in cats with chronic kidney disease. J Vet Intern Med 2007, 21: 906-916.
27. Lund EM, Armostrong PJ, Kirk CA, Kolar LM, Klausner JS. Health status and population characteristics of dogs and cats examined at private veterinary practices in the United States. J Am Vet Med Assoc 1999, 214: 1336-1341.
28. Watson A. Indicators of renal insufficiency in dogs and cats presented at a veterinary teaching hospital. Austral Vet Pract 2001, 31: 54-58.
29. White JD, Norris JM, Baral RM, Malik R. Naturally – occurring chronic renal disease in Australian cats: a prospective study of 184 cases. Austr Vet J 2006, 84: 188-194.
30. Heiene R, Rumsby G, Ziener M, Dahl SA, Tims C, Teiqe J, Ottesen N. Chronic kidney disease with three cases of oxalate-like nephrosis in Ragdoll cats. J Feline Med Surg 2009, 11: 474-480.
31. Syme HM, Barber PJ, Markwell PJ, Elliott J. Prevalence of systolic hypertension in cats with chronic renal failure at initial evaluation. J Am Vet Med Assoc 2002, 220: 1799-1804.
32. Syme HM, Markwell PJ, Pfeiffer D, Elliott J. Survival of cats with naturally occurring chronic renal failure is related to severity of proteinuria. J Vet Intern Med 2006, 20: 528-535.
33. Jepson RE, Brodbelt D, Vallance C, Syme HM, Elliott J. Evaluation of predictors of the development of azotemia in cats. J Vet Intern Med 2009, 23: 806-813.
34. Mayer-Roenne B, Goldstein RE, Erb HN. Urinary tract infections in cats with hyperthyroidism, diabetes mellitus and chronic kidney disease. J Feline Med Surg 2007, 9: 124-132.
35. Miyagawa Y, Takemura N, Hirose H. Assessments of factors that affect glomerular filtration rate and internal markers of renal function in dogs and cats. J Vet Med Sci 2010, 72: 1129-1136.
36. Kobayashi DL, Peterson ME, Graves TK, Lesser M, Nichols CE. Hypertension in cats with chronic renal failure or hyperthyroidism. J Vet Intern Med 1990, 4: 58- 62.
37. Stiles J, Polzin DJ, Bistner SI. The prevalence of retinopathy in cats with systemic hypertension and chronic renal failure or hyperthyroidism. J Am Anim Hosp Assoc 1994, 30: 564-572.
38. Jepson R. Feline systemic hypertension. Classification and pathogenesis. J Feline Med Surg 2011, 13: 25-34.
39. White JD, Malik R, Norris JM, Malkides N. Association between naturally occurring chronic kidney disease and feline immunodeficiency virus infection status in cats. J Am Vet Med Assoc 2010, 236: 424-429.
40. Barber P, Miller JB, Rand J. The thin, inappetent cat. In: Problem-Based Feline Medicine. Rand J (ed). Elsevier Saunders: Edinburgh, 2006, pp. 330-363.
41. Jensen J, Henik RA, Brownfield M, Armstrong J. Plasma renin activity and angiotensin I and aldosterone consentrations in cats with hypertension associated with chronic renal disease. Am J Vet Res 1997, 58: 535- 540.
42. Elliott J, Rawlings JM, Markwell PJ, Barber PJ. Survival of cats with naturally occurring chronic renal failure: effect of dietary management. J Small Anim Pract 2000, 41: 235-242.
43. Barber PJ, Rawlings JM, Markwell PJ, Elliott J. Effect of dietary phosphate restriction on renal secondary hyperparathyroidism in the cat. J Small Anim Pract 1999, 40: 62-70.
44. Polzin DJ, Osborne CA, Ross S, Jacob F. Dietary management of feline chronic renal failure: where are we now? In what direction are we headed? J Feline Med Surg 2000, 2: 75-82.
45. Wills SJ, Barrett EL, Barr FJ, Bradley KJ, Helps CR, Cannon MJ, Gruffydd-Jones TJ. Evaluation of the repeatability of ultrasound scanning for detection of feline polycystic kidney disease. J Feline Med Surg 2009, 11: 993-996.



