Γρουτίδου Α. Kτηνίατρος, Κλινική Ζώων Συντροφιάς, Τμήμα Κτηνιατρικής, Α.Π.Θ., Θεσσαλονίκη | Νικάνδρου Μ. Ε. Kτηνίατρος, Κλινική Ζώων Συντροφιάς, Τμήμα Κτηνιατρικής, Α.Π.Θ., Θεσσαλονίκη | Σαρπεκίδου Ε. Kτηνίατρος, υποψήφια Διδάκτορας, Κλινική Ζώων Συντροφιάς, Τμήμα Κτηνιατρικής, Α.Π.Θ., Θεσσαλονίκη | Καζάκος Γ. Κτηνίατρος, PhD, Κλινική Ζώων Συντροφιάς, Τμήμα Κτηνιατρικής, Α.Π.Θ., Θεσσαλονίκη
Λέξεις ευρετηρίου: κακώσεις θωρακοσφυϊκής μοίρας νωτιαίου μυελού, παραπληγία, φυσικοθεραπεία, γεννήτορας κεντρικών προτύπων της κίνησης
Περίληψη
Η νωτιαία βάδιση (ΝΒ) είναι η ανάπτυξη ακούσιας κινητικότητας σε σκύλους και γάτες, οι οποίοι έπειτα από οξεία κάκωση στην θωρακοσφυϊκή (ΘΟ) χώρα παρέμειναν παραπληγικοί και χωρίς εν τω βάθει αίσθηση του άλγους στα οπίσθια άκρα. Η ΝΒ είναι κλινικά σημαντική αφού ευνοεί τις εναλλακτικές επιλογές εκτός της ευθανασίας στα ζώα αυτά.
Σκοπός του παρόντος άρθρου είναι η παρουσίαση των χαρακτηριστικών του ζώου και των ευρημάτων της κλινικής και νευρολογικής εξέτασης που είναι συμβατά με αυξημένες πιθανότητες ανάπτυξης ΝΒ, αλλά και τα μέτρα που μπορεί να λάβει ο κτηνίατρος και ο κηδεμόνας του ζώου με σκοπό την επίτευξή της.
Φαίνεται πως ελαφρύτερα, νεαρότερα ζώα, με αυξημένο τόνο οπισθίων άκρων είναι πιο πιθανό να αναπτύξουν ΝΒ. Αν και η ΝΒ προκύπτει αυτόματα, η εισαγωγή του ζώου σε ένα πρόγραμμα φυσικής αποκατάστασης μπορεί να προετοιμάσει ένα ισχυρό μυοσκελετικό σύστημα που να μπορεί να υποστηρίξει την πιθανή επερχόμενη ανάπτυξη της ΝΒ. Παραδοσιακές τεχνικές είναι το παθητικό εύρος κίνησης, η κινησιοθεραπεία και η μάλαξη των μυών και σε συνδυασμό με ηλεκτροδιέγερση μπορούν να ωφελήσουν στο μέγιστο το ζώο.
Στην βιβλιογραφία αναφέρονται ποσοστά επιτυχίας στην επίτευξη ΝΒ 10-59% στους σκύλους με το διάμεσο χρόνο να ποικίλει από 75 μέρες μέχρι 28 μήνες. Μεγαλύτερα ποσοστά επιτυχίας και μικρότεροι διάμεσοι χρόνοι παρατηρήθηκαν σε ζώα τα οποία υποβλήθηκαν σε φυσικοθεραπεία. Στις γάτες, το ποσοστό αυτό κυμαίνεται από 0-45%, με το ψηλότερο ποσοστό να αντιστοιχεί στις γάτες οι οποίες υποβλήθηκαν σε φυσικοθεραπεία και ο μέσος όρος του μεσοδιαστήματος εμφάνισης νωτιαίας βάδισης στις μελέτες αυτές είναι 47 μέρες.
Ένα ζώο το οποίο έχει υποστεί οξεία κάκωση του νωτιαίου μυελού, παραπληγία και απώλεια της εν τω βάθει αίσθησης του άλγους δεν πρέπει να καταδικάζεται. Η ΝΒ μπορεί υπό προϋποθέσεις και με την βοήθεια ενός αποφασισμένου κηδεμόνα να παράσχει μια αποδεκτή ποιότητα ζωής στο ζώο.
Εισαγωγή
Οι οξείες κακώσεις της θωρακοσφυϊκής (ΘΟ) μοίρας του νωτιαίου μυελού (ΝΜ) είναι συχνές στα ζώα συντροφιάς, και οι συνέπειές τους πολλές φορές μπορεί να είναι σοβαρές (Granger & Carwardine 2014). Ενδέχεται να προκληθούν από προβολή μεσοσπονδύλιου δίσκου (ΠΜΔ), κάταγμα/υπεξάρθρημα σπονδύλων, τραύμα από ξένο σώμα ή άλλα αίτια συμπίεσης και θλάσης του ΝΜ (Olby & Jeffery 2012). Η επιλογή της ευθανασίας ως διαχείριση είναι συχνή σε τέτοια περιστατικά, καθώς σε απουσία της εν τω βάθει αίσθησης του άλγους (ΕΒΑΑ) η πρόγνωση θεωρείται δυσμενής (Olby et al. 2020). Όμως, σύμφωνα με μελέτες (Gallucci et al. 2017, Lewis et al. 2020) μπορεί να αναπτυχθεί νωτιαία βάδιση (ΝΒ), ένα είδος αντανακλαστικού βαδίσματος που απασχολεί την παρούσα ανασκόπηση.
Η ΝΒ είναι η ανάπτυξη ακούσιας κινητικότητας των οπισθίων άκρων σε σκύλους και γάτες που παρέμειναν παραπληγικοί και χωρίς ΕΒΑΑ έπειτα από οξεία κάκωση στην ΘΟ μοίρα του ΝΜ (Gallucci et al. 2017). Πιο συγκεκριμένα, είναι ένα είδος αντανακλαστικού βαδίσματος που αναπτύσσεται χάρη σε περίπλοκες δυναμικές αλληλεπιδράσεις μεταξύ του γεννήτορα κεντρικών προτύπων (ΓΚΠ) της κίνησης των οπισθίων άκρων (pelvic limb locomotor central pattern generator, CPG) και της ιδιοδεκτικής ανατροφοδότησης από τα άκρα, όταν έχει απωλεσθεί ο ανώτερος έλεγχος του εγκεφάλου επί του ΝΜ λόγω κάκωσης του τελευταίου (Gallucci et al. 2017). Ανάκτηση κάποιου βαθμού κινητικής δραστηριότητας έπειτα από κάκωση του ΝΜ εκτός από τον σκύλο και την γάτα, έχει παρατηρηθεί και σε άλλα είδη ζώων όπως μαϊμούδες, αρουραίους, κονίκλους, οπόσουμ, περιστέρια και βάτραχους (Rossignol et al. 1996).
Το παρόν άρθρο, θα επικεντρωθεί στα περιστατικά με κάκωση της ΘΟ μοίρας του ΝΜ που έχουν απωλέσει την ΕΒΑΑ. Σκοπός της παρούσας μελέτης είναι η περιγραφή του φαινομένου της ΝΒ, τα κλινικά της χαρακτηριστικά και η κλινική της σημασία.

►Βίντεο 1. Παραπληγική γάτα κατά τη διάρκεια φυσικοθεραπείας σε κυλιόμενο διάδρομο που ανέπτυξε νωτιαία βάδιση.
Η ΝΒ χαρακτηρίζεται κλινικά από έλλειψη συντονισμού των οπισθίων άκρων ως προς τα πρόσθια, δυσκολία των οπισθίων άκρων κατά την αλλαγή κατεύθυνσης του σώματος, δυσκολία στην κίνηση προς τα πίσω, καθώς και από συχνές πτώσεις. Οι πτώσεις αυτές παρατηρούνται κυρίως κατά τις στροφές και συνήθως προς την μία πλευρά, αν και κάποια ζώα έχουν την τάση να προσπαθούν να αποφύγουν την πτώση λόγω της αυξημένης σπαστικότητας του σύστοιχου άκρου. Σε ορισμένες περιπτώσεις, τα ζώα μπορεί να είναι ανίκανα να πραγματοποιήσουν κίνηση από μόνα τους, όμως το επιτυγχάνουν αν προκληθεί ερεθισμός της περινεϊκής χώρας με νύξη της περιοχής (Lovely et al. 1986, Rossignol et al. 1999). Παρόλα αυτά, αρκετά ζώα έχουν την ικανότητα να περπατούν για τουλάχιστον 10 βήματα, χωρίς βοήθεια και χωρίς πτώσεις. Κατά τη διάρκεια της βάδισης, μπορεί να παρατηρηθούν διάφορα είδη κίνησης των οπισθίων άκρων. Δηλαδή, κάποια ζώα λόγω της σπαστικότητας των καμπτήρων μυών εμφανίζουν υπερμετρία, ενώ σε άλλα ζώα παρατηρείται βάδιση και στήριξη στη ραχιαία επιφάνεια των δακτύλων (knuckling) των οπισθίων άκρων στο έδαφος. Επίσης, ζώα με ΝΒ συνήθως κατά την προσπάθειά τους να έρθουν σε όρθια θέση στηρίζουν το βάρος τους κυρίως στο πρόσθια άκρα. Επιπρόσθετα, μερικές μέρες μετά την οξεία κάκωση συχνά παρατηρούνται διαταραχές των αντανακλαστικών, όπως για παράδειγμα το παθολογικό αντανακλαστικό της υπερέκτασης του ετερόπλευρου οπίσθιου άκρου κατά την εκτέλεση του αντανακλαστικού της κάμψης (cross extensor reflex) (Lewis et al. 2020) (►Βίντεο 1) (►Βίντεο 2) (►Βίντεο 3).
Κλινική εικόνα
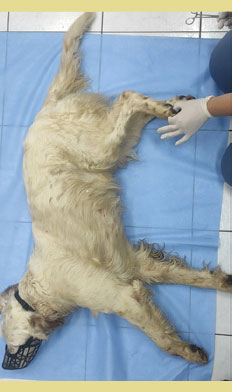
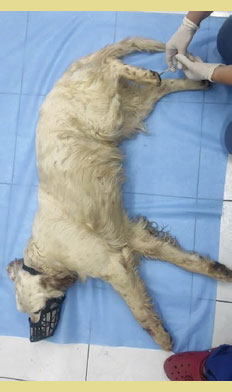
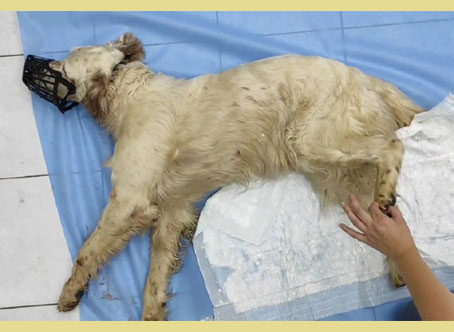
Αρχικά, κατά την προσκόμιση των ζώων αυτών στην κλινική (και πριν φυσικά αναπτυχθεί η ΝΒ) παρατηρείται παράλυση των οπισθίων άκρων και απώλεια της ΕΒΑΑ στα δύο οπίσθια άκρα (Fitzmaurice 2010, Gallucci et al. 2017).
Κατά τη διάρκεια της νευρολογικής εξέτασης ενός ζώου που έχει αναπτύξει ΝΒ αρχικά θα παρατηρηθεί η μη φυσιολογική βάδιση με αταξία και παραπάρεση, όπως αναφέρθηκε ανωτέρω. Ακολούθως παρατηρείται διαταραχή της ιδιοδεκτικής αισθητικότητας η οποία μπορεί να εκδηλωθεί με διάφορους τρόπους όπως καθυστερημένη ανταπόκριση στη δοκιμή μετακίνησης στο ένα άκρο και μη ανταπόκριση στη δοκιμή υπερέκτασης και οπισθοδρόμισης στο οπίσθια άκρα. Aξίζει να αναφερθεί πως η δοκιμή της επαναφοράς του άκρου μπορεί να είναι φυσιολογική. Όσο αφορά τα νωτιαία αντανακλαστικά, είναι συνήθως αυξημένα, όπως και αυξημένη είναι συχνά η σπαστικότητα των εκτείνοντων και καμπτήρων μυών. Επίσης παρατηρούνται ταυτόχρονα αντανακλαστικές κινήσεις των μυών που αντιστοιχούν σε νευροτόμια του ΝΜ οπισθίως της θέσης κάκωσής του (mass reflex): ακούσιοι σπασμοί των καμπτήρων μυών των οπισθίων άκρων, αντανακλαστική ανόρθωση της ουράς, κένωση της ουροδόχου κύστης ή του κόλου κατά την απτική ή άλλη αισθητική διέγερση (πχ. άσκηση πίεσης για κένωση της ουροδόχου κύστης) (Lewis et al. 2020).
Πρέπει να σημειωθεί πως πολύ συχνά κατά την νευρολογική εξέταση, το θετικό αντανακλαστικό της κάμψης λαμβάνεται λανθασμένα ως ΕΒΑΑ, επομένως είναι απαραίτητο να διαχωριστούν αυτά τα δύο φαινόμενα. Η ύπαρξη θετικού αντανακλαστικού της κάμψης, δεν υποδεικνύει ότι ένα ζώο έχει ΕΒΑΑ (Fitzmaurice 2010) (►Βίντεο 4). H απλή κάμψη του άκρου είναι απόδειξη ότι οι κάτω κινητικοί νευρώνες είναι άθικτοι, γεγονός που επιτρέπει την λειτουργία του αντανακλαστικού, χωρίς να δίνεται όμως πληροφορία για την ΕΒΑΑ, η οποία προϋποθέτει επικοινωνία με τα ανώτερα κέντρα ελέγχου και άρα δεν εγγυάται από την ακεραιότητα μόνο των κάτω κινητικών νευρώνων (ΚΚΝ) (Fitzmaurice 2010, De Lahunta et al. 2021). Η ΕΒΑΑ ελέγχεται με την άσκηση επώδυνου ερεθίσματος όπως η νύξη ενός μεσοδακτύλιου διαστήματος ή μίας φάλαγγας με αιμοστατική λαβίδα (Garosi 2004) (►Βίντεο 5). Η δοκιμή θεωρείται θετική όταν το ζώο εκφράζει συνειδητή - συμπεριφορική αντίδραση, δηλαδή στροφή κεφαλής προς το ερέθισμα, προσπάθεια δαγκώματος ή κραυγή (Garosi 2004) (►Βίντεο 6). Είναι σημαντικό να ελέγχονται τόσο τα έσω όσο και τα έξω δάχτυλα όλων των άκρων, καθώς αναλόγως των ευρημάτων μπορούν να εξαχθούν πληροφορίες για την εντόπιση της βλάβης (Añor 2004). Επιπλέον ελέγχεται και η αισθητικότητα στην βάση της ουράς, έτσι ώστε να βεβαιωθεί κανείς πως ένα ζώο δεν έχει ΕΒΑΑ. Η συνειδητή αντίδραση του ζώου σε οποιοδήποτε από τα παραπάνω ερεθίσματα συνεπάγεται την παρουσία ΕΒΑΑ (Olby et al. 2020). Επομένως, η επιβεβαίωση ότι ένα ζώο έχει ΝΒ και όχι αταξία/ πάρεση άλλης αιτιολογίας, είναι η απουσία της ΕΒΑΑ.
►Βίντεο 6. Θετικό αντανακλαστικό κάμψης οπίσθιου άκρου και αρνητικός έλεγχος εν τω βάθει αισθητικότητας στο ίδιο άκρο, σε παραπληγικό σκύλο. Θετικός έλεγχος εν τω βάθει αισθητικότητας στο φυσιολογικό πρόσθιο άκρο.
Παθοφυσιολογία
Παρόλο που ως γνωστόν το κεντρικό νευρικό σύστημα έχει μικρή αναγεννητική ικανότητα, εμφανίζει εντυπωσιακή πλαστικότητα (Lewis et al. 2020). Πλαστικότητα λέγεται η αναδιοργάνωση των διασωθέντων νευρώνων σε λειτουργικό κύκλωμα που μπορεί να συνεχίσει να συμβαίνει ακόμα και εβδομάδες ή μήνες μετά την κάκωση (Jeffery & Blakemore 1999). Μελέτες συνηγορούν ότι η ανάκτηση της βάδισης μπορεί να προκύψει μέσω διαδικασιών όπως: α. αναγέννηση των νευραξόνων στο σημείο τραυματισμού, β. επαναφορά της λειτουργίας ανέπαφων νευραξόνων άνω κινητικών νευρώνων (ΑΚΝ) που διασχίζουν το σημείο τραυματισμού, γ. πιο αυτόνομος ρόλος του γεννήτορα κεντρικών προτύπων (CPGs), δ. μεταβολές στην διεγερσιμότητα των διάμεσων νευρώνων και ΚΚΝ οπισθίως του σημείου βλάβης, ε. ενεργοποίηση «σιωπηλών» συνάψεων, στ. αλλαγής της «βαρύτητας» (ή δυναμικής) κάποιων συνάψεων, ζ. μεταβολές στην αντίληψη αισθητικών ερεθισμάτων στα επίπεδα του ΝΜ οπισθίως της βλάβης (Lewis et al. 2020, De Lahunta et al. 2021).
Περαιτέρω επεξήγηση απαιτείται όσον αφορά τα CPGs. Καταρχάς, τα CPGs είναι αυτοτελή νευρωνικά κυκλώματα που παράγουν επαναλαμβανόμενα μοτίβα κινητικής συμπεριφοράς ανεξαρτήτως αισθητικής διέγερσης ή ανατροφοδότησης (Bucher2009). Τα κυκλώματα αυτά υπάρχουν εκτός των άλλων και στον NM και συμβάλλουν στην δημιουργία κίνησης από τα οπίσθια άκρα (Lewis et al. 2020). Τα CPGs θεωρητικά εκτείνονται κατά μήκος όλου του ΝΜ, αλλά κυρίως έχουν μελετηθεί αυτά που βρίσκονται στην οσφυϊκή μοίρα του και αφορούν στα οπίσθια άκρα (Lewis et al. 2020). Έχουν την ικανότητα να δημιουργούν ένα βασικό μοτίβο βάδισης, καθώς και να συντονίζουν το δεξί με το αριστερό άκρο (Lewis et al. 2020). Η κίνηση αυτή μπορεί να δημιουργηθεί ανεξάρτητα από την επικοινωνία με τον εγκέφαλο και επιτυγχάνεται μέσω της συνεργασίας διάμεσων νευρώνων (νευρώνες οι οποίοι μεταδίδουν ερεθίσματα μεταξύ άλλων νευρώνων) και ΚΚΝ οι οποίοι νευρώνουν τους σκελετικούς μύες (Lewis et al. 2020). Ενώ σε φυσιολογικά ζώα τα CPGs υπόκεινται στον έλεγχο του εγκεφάλου για την έναρξη της δραστηριότητάς τους, σε ζώα με κακώσεις της ΘΟ μοίρας έχει αποδειχθεί πως αποκτούν μεγαλύτερη αυτονομία, συμβάλλοντας στη ΝΒ (Lewis et al. 2020). Συμπερασματικά, η ενεργοποίηση των CPGs, φαίνεται να υποβοηθάται από την λειτουργία των διάμεσων νευρώνων του ΝΜ, από τις μεταβολές στην διεγερσιμότητα των κινητικών νευρώνων και από την μεταβολή στην αντίληψη των αισθητικών ερεθισμάτων (Lewis et al. 2020).
Η ΕΒΑΑ είναι ο πιο σημαντικός έμμεσος προγνωστικός δείκτης της ανάκτησης εκούσιας περιπατητικότητας σε περίπτωση κάκωσης του ΝΜ καθώς σε απουσία της οι πιθανότητες για πλήρη ανάκτηση εκούσιας κίνησης είναι εξαιρετικά μειωμένες (Olby et al. 2004). Για να γίνει κατανοητή η εξήγηση αυτού του φαινομένου, πρέπει πρώτα να αναφερθεί πως οι μεγάλου μεγέθους εμμύελες νευρικές ίνες που σχηματίζουν τα δεμάτια που συμμετέχουν στη βάδιση, είναι πιο ευαίσθητες στην κάκωση συγκριτικά με τις μικρού μεγέθους αμύελες νευρικές ίνες (Sharp & Wheeler 2005). Οπότε όταν η βλάβη αφορά μέχρι και τις ανθεκτικές αμύελες ίνες, γεγονός που γίνεται αντιληπτό από την έλλειψη ΕΒΑΑ, θεωρείται πως η νευρολογική βλάβη είναι πολύ βαριά (Sharp & Wheeler 2005). Επιπλέον, οι νευράξονες των νευρώνων που είναι υπεύθυνοι για την ΕΒΑΑ πορεύονται στην εσωτερική επιφάνεια της πλάγιας δέσμης της λευκής ουσίας του ΝΜ, δηλαδή στα ενδότερα σημεία του, σχηματίζοντας το νωτιαιοθαλαμικό δεμάτιο (Schatzberg et al. 2012). Άρα, σε περίπτωση βαριάς βλάβης αυτών των νευραξόνων, σημαίνει πως συνυπάρχει και βαριά βλάβη στους νευρώνες των περιφερικότερων δεματίων (που είναι εμμύελοι) και είναι υπεύθυνοι για την βάδιση (Schatzberg et al. 2012). Ως εκ τούτου, σε τέτοια ζώα οι πιθανότητες για ανάκτηση της ΕΒΑΑ και της βάδισης είναι λιγότερες (Schatzberg et al. 2012).
Αξίζει να αναφερθεί ότι σε σκύλους με ΠΜΔ τύπου Ι κατά Hansen και επακόλουθη απώλεια της ΕΒΑΑ, έπειτα από επέμβαση αποσυμπίεσης, ανακτήθηκε η ΕΒΑΑ και η ικανότητα βάδισης σε ποσοστό 58% (Olby et al. 2003). Αντίθετα, σκύλοι με ΠΜΔ τύπου Ι κατά Hansen, χωρίς απώλεια ΕΒΑΑ, έπειτα από επέμβαση είχαν ποσοστά επιτυχίας 72100% (Kerwin et al. 2012).
Προδιαθέτοντες παράγοντες ανάπτυξης νωτιαίας βάδισης
Πρέπει να αναφερθεί πως η πλειονότητα των κλινικών πληροφοριών για τους σκύλους προέρχεται από περιστατικά ΠΜΔ τύπου Ι κατά Hansen, καθώς είναι η πιο συχνή πάθηση του ΝΜ σε αυτό το είδος (Granger & Carwardine 2014). Αντίθετα, η πιο συχνή αιτιολογία μυελοπάθειας στις γάτες είναι η τραυματική (Granger & Carwardine 2014). Επίσης, στις γάτες υπάρχει έλλειψη βιβλιογραφίας όσον αφορά στους φυσικά προκαλούμενους τραυματισμούς, αφού, εκτός από την έρευνα των Gallucci et al (2021), οι περισσότερες έρευνες είναι πειραματικές (Gallucci et al. 2021).
1. Χαρακτηριστικά ζωών
Σε μία έρευνα, το σωματικό βάρος των σκύλων φαίνεται να είναι σημαντικό, καθώς μικρότερου μεγέθους σκύλοι και συγκεκριμένα κάτω των 7,8 κιλών, εμφανίζουν περισσότερες πιθανότητες ανάπτυξης ΝΒ (Gallucci et al. 2017). Εικάζεται ότι ίσως είναι πιο εύκολο για τους μικρόσωμους σκύλους να μεταφέρουν παραπάνω βάρος στα πρόσθια άκρα, «αποφορτίζοντας» έτσι τα οπίσθια, πιο αδύναμα άκρα (Lewis et al. 2020). Αντίθετα, ίσως είναι πιο δύσκολο για τους ψηλότερους σκύλους, με πιο υψηλό κέντρο βάρους να έχουν καλή ισορροπία, εμποδίζοντάς τους να ανακτήσουν ικανότητα βάδισης (Lewis et al. 2020). Ακολούθως, με βάση την έρευνα των Gallucci et al (2017), φαίνεται πως νεότεροι σκύλοι, κάτω των 60 μηνών, είναι πιο πιθανό να αναπτύξουν ΝΒ, αν και άλλες έρευνες έδειξαν πως η ηλικία είναι άνευ σημασίας (Jeffery et al. 2016) ή πως η νεότερη ηλικία σχετίζεται μόνο με την πιο γρήγορη ανάπτυξη NB (Olby et al. 2003). Πρέπει να σημειωθεί όμως, πως στην έρευνα των Gallucci et al (2017), οι σκύλοι αυτοί είχαν υποβληθεί σε φυσικοθεραπεία, γεγονός το οποίο επηρεάζει την έκβαση. Σχετικά με τις γάτες, μία πειραματική έρευνα έδειξε πως παραπληγικά γατάκια 2 εβδομάδων είχαν μεγαλύτερη πιθανότητα ανάπτυξης ΝΒ από παραπληγικές γάτες 12 εβδομάδων (Smith et al. 1982). Συγκεκριμένα, στην εν λόγω μελέτη όλα τα γατάκια 2 εβδομάδων ανέπτυξαν ΝΒ, ανεξαρτήτως του αν υποβλήθηκαν ή όχι σε φυσικοθεραπεία (Smith et al. 1982). Αντιθέτως, μόνο οι 3 από τις 5 γάτες 12 εβδομάδων που υποβλήθηκαν σε φυσικοθεραπεία ανέπτυξαν ΝΒ, ενώ όσες δεν υποβλήθηκαν δεν ανέπτυξαν ΝΒ (Smith et al. 1982).
2. Κλινική εικόνα
Η ύπαρξη των ακόλουθων κλινικών σημείων κατά την προσκόμιση ενδεχομένως να μπορεί να δώσει στοιχεία για τη πιθανότητα ανάπτυξης ΝΒ. Αρχικά, σύμφωνα με την έρευνα των Lewis & Olby (2017) ιδιαίτερη σημασία φαίνεται να έχει η αυξημένη διάρκεια σπασμού των καμπτήρων μυών των οπισθίων άκρων, καθώς υπάρχει θετική συσχέτιση μεταξύ αυτής και της ανάπτυξης κάποιου είδους βάδισης. Οι σπασμοί αυτοί προκλήθηκαν έπειτα από νύξη με καρφίτσα στο κάτω μέρος του ποδιού (Lewis & Olby 2017). Παρόλα αυτά, το εν λόγω πείραμα πραγματοποιήθηκε σε ζώα τα οποία είχαν υποστεί οξεία κάκωση του ΝΜ τουλάχιστον 3 μήνες πριν και με σταθερή κλινική εικόνα, συνεπώς είναι πιθανό η αυξημένη διάρκεια του σπασμού των καμπτήρων μυών των οπισθίων άκρων να μην μπορεί να χρησιμοποιηθεί ως προγνωστικός δείκτης σε πιο πρόσφατα περιστατικά (Lewis & Olby 2017).
Όσον αφορά στις γάτες, σύμφωνα με την έρευνα των Gallucci et al. (2021), η ύπαρξη του παθολογικού αντανακλαστικού της υπερέκτασης του ετερόπλευρου οπισθίου άκρου κατά την εκτέλεση του αντανακλαστικού της κάμψης (cross extensor reflex) κατά την προσκόμιση, βρέθηκε να έχει θετική συσχέτιση με την ανάπτυξη ΝΒ (Gallucci et al. 2021).
Αξίζει να σημειωθεί πως η ανάκτηση κινητικής δραστηριότητας στον σκύλο παρατηρείται πιο σπάνια σε περιστατικά κάκωσης της σπονδυλικής στήλης τραυματικής αιτιολογίας (Olby et al. 2003). Αυτό μπορεί να οφείλεται στο ότι σε τέτοιες περιπτώσεις συνήθως προκαλούνται πιο εκτεταμένες ή πολλαπλές κακώσεις, καθώς και διατομή του ΝΜ ή στο ότι σε τέτοιες περιπτώσεις επιλέγεται πιο συχνά η ευθανασία (Olby et al. 2003, Lewis et al. 2020). Άξιο αναφοράς είναι επίσης το γεγονός ότι κακώσεις οπισθίως της ΘΟ μοίρας του ΝΜ δεν καταλήγουν σε ΝΒ, αφού τότε επέρχεται βλάβη στο ίδιο το CPG (De Lahunta et al. 2021).
Όσον αφορά στις γάτες, δεν έχει βρεθεί συσχέτιση μεταξύ του επιπέδου της βαρύτητας των συμπτωμάτων και της ανάπτυξης ή όχι ΝΒ (Gallucci et al. 2021).
3. Εργαστηριακές εξετάσεις
Έχουν γίνει προσπάθειες να προσδιοριστούν παράμετροι του αίματος και του εγκεφαλονωτιαίου υγρού οι οποίες θα μπορούσαν να χρησιμοποιηθούν ως προγνωστικοί δείκτες της έκβασης των περιστατικών ζώων χωρίς ΕΒΑΑ, χωρίς όμως αποτέλεσμα (Olby et al. 2020).
Συχνότητα και χρόνος εμφάνισης νωτιαίας βάδισης
Τα ποσοστά των σκύλων που κατάφεραν να αναπτύξουν ΝΒ έπειτα από φυσικά προκαλούμενη βλάβη της ΘΟ μοίρας του ΝΜ και απώλεια της ΕΒΑΑ παρουσιάζουν μεγάλο εύρος και συγκεκριμένα κυμαίνονται από 10% έως 59%. Αυτό ίσως οφείλεται στις διαφορές που εντοπίζονται στον πληθυσμό, στο είδος των κακώσεων και στην πιθανότερη επιλογή της ευθανασίας στις τραυματικής αιτιολογίας κακώσεις (Olby et al. 2003, Gallucci et al. 2017, Hu et al. 2018, Lewis et al. 2019, Lewis et al. 2020). Αξίζει να αναφερθεί σε αυτό το σημείο πως το ψηλότερο ποσοστό ανάπτυξης ΝΒ (59%), παρατηρήθηκε σε έρευνα όπου οι σκύλοι υποβλήθηκαν σε εντατική φυσικοθεραπεία (Gallucci et al. 2017). Όσον αφορά την ΠΜΔ τύπου Ι κατά Hansen, το ποσοστό των σκύλων που κατάφεραν να αναπτύξουν ΝΒ ήταν 18% - 31% (Olby et al. 2003, Aikawa et al. 2012).
Ο διάμεσος χρόνος εμφάνισης ΝΒ στον σκύλο παρουσιάζει μεγάλη διακύμανση. O διάμεσος χρόνος εμφάνισης σε μία έρευνα ήταν 9 μήνες (εύρος: από 4 έως 18 μήνες) ενώ σε μία δεύτερη έρευνα στην οποία οι ασθενείς υποβλήθηκαν σε φυσικοθεραπεία, διάμεσος χρόνος εμφάνισης ήταν μόλις 75 μέρες (εύρος: από 16 έως 350 μέρες) (Olby et al. 2003, Gallucci et al. 2017). Σε περιστατικά ΠΜΔ τύπου Ι κατά Hansen, ο διάμεσος χρόνος εμφάνισης ΝΒ ήταν επίσης 9 μήνες, με εύρος από 2 έως 28 μήνες (Olby et al. 2003, Aikawa T et al. 2012).
Στις γάτες, στην μοναδική κλινική μελέτη διαθέσιμη στη βιβλιογραφία που καταγράφονται περιστατικά με φυσικούς τραυματισμούς, καμία από τις 7 γάτες δεν κατάφερε να αναπτύξει ΝΒ (Gallucci et al. 2021). Αντιθέτως, σε 2 πειραματικές έρευνες, βρέθηκε πως το 83%-87,5% γατών ανέπτυξαν ΝΒ (Lovely et al. 1986, De Leon et al. 1998).
Μυελομαλάκυνση
Σκύλοι με απώλεια ΕΒΑΑ κινδυνεύουν να εμφανίσουν μυελομαλάκυνση, για την οποία δεν υπάρχει θεραπεία και οδηγεί συνήθως στο θάνατο του ζώου (Castel et al. 2019). Έχει βρεθεί πως τα ποσοστά μυελομαλάκυνσης λόγω ΠΜΔ τύπου I κατά Hansen σε σκύλους χωρίς ΕΒΑΑ κυμαίνονται από 9 έως 33% (Olby et al. 2020). Τα κλινικά σημεία της μυελομαλάκυνσης μπορεί να υπάρχουν ήδη κατά τη προσκόμιση ή να αναπτυχθούν έως 5 μέρες μετά (Castel et al. 2017). Στην επέκταση ουραίως παρατηρείται απώλεια των νωτιαίων αντανακλαστικών των οπίσθιων άκρων, μειωμένος τόνος των κοιλιακών τοιχωμάτων, μειωμένο ή απών περινεϊκό αντανακλαστικό και μειωμένος ή απόν τόνος του πρωκτού (Castel et al. 2017). Καθώς η μυελομαλάκυνση επεκτείνεται προς τη θωρακική και αυχενική μοίρα του ΝΜ, παρατηρείται αναπνευστική δυσχέρεια λόγω παράλυσης των μεσοπλεύριων μυών, χάνονται τα νωτιαία αντανακλαστικά των προσθίων άκρων, παρουσιάζεται αμφοτερόπλευρο σύνδρομο Horner και τέλος θάνατος (Castel et al. 2019).
Υποστηρικτικά μετρά του παραπληγικού ζώου με απώλεια της εν τω βάθει αισθητικότητας του άλγους
Όπως ήδη αναφέρθηκε, το ΚΝΣ χαρακτηρίζεται από πλαστικότητα, και ως εκ τούτου έχει τη δυνατότητα μέσω διαφόρων μηχανισμών να αμβλύνει τις επιπτώσεις από βλάβες που προκύπτουν. Μέσω της πλαστικότητας, και με τη βοήθεια επαναλαμβανόμενης εξωτερικής διέγερσης, οι εναπομείναντες νευρώνες αποκτούν ουσιαστικά νέες λειτουργίες, με αποτέλεσμα να υπάρχει η πιθανότητα αποκατάστασης ακόμα και σε σοβαρές κακώσεις του νωτιαίου μυελού (Sherman & Olby 2004). Όπως είναι γνωστό, η μη χρήση των άκρων οδηγεί σε απώλεια μυϊκής μάζας, μόνιμες συσπάσεις μυϊκών ομάδων και αλλοίωση των αρθρώσεων και των σχετικών δομών (αγκυλώσεις). Η φυσικοθεραπεία θεωρείται κρίσιμη στην αναχαίτιση αυτών των φαινομένων και στην επίτευξη της μέγιστης δυνατής αποκατάστασης (Sherman & Olby 2004).
Μέχρι τώρα, υπάρχουν περιορισμένες κλινικές μελέτες που να αναπτύσσουν και να αποδεικνύουν την αποτελεσματικότητα συγκεκριμένων θεραπευτικών παρεμβάσεων στην ανάπτυξη ΝΒ όσον αφορά σκύλους χωρίς ΕΒΑΑ (Lewis et al. 2020). Ωστόσο, πληροφορίες από πειραματικά μοντέλα και τραυματισμούς σπονδυλικής στήλης ανθρώ- πων μπορεί να φανούν χρήσιμες για εφαρμογή και στους σκύλους.
Για να επιλεχθεί το πιο κατάλληλο πρόγραμμα αποκατάστασης για το κάθε ζώο, πρέπει να ληφθούν υπόψιν η ικανότητα περιπατητικότητας και η παρουσία άλλων προβλημάτων υγείας. Σε κάθε περίπτωση, το πλάνο πρέπει να τηρεί τους εξής κανόνες:
1. Ύπαρξη υποστηρικτικής φροντίδας για πρόληψη δευτερευόντων προβλημάτων και παροχή του κατάλληλου περιβάλλοντος για αποκατάσταση.
2. Προσπάθεια αναχαίτισης της εξέλιξης της βλάβης εντός του νευρικού συστήματος.
3. Διατήρηση της μυϊκής μάζας και του εύρους της κίνησης, μεγιστοποίηση της πλαστικότητας εντός του νευρικού συστήματος και διέγερση των ιδιοδεκτικών νευρικών οδών προς επανεκμάθηση του φυσιολογικού βαδίσματος (Sherman & Olby 2004).
Ούρηση
Κάκωση στη ΘΟ μοίρα της σπονδυλικής στήλης, που θα καταλήξει σε ΝΒ, θα έχει και επακόλουθη δυσλειτουργία της ουροδόχου κύστης, λόγω βλάβης των ΑΚΝ των σφιγκτήρων, συνεχούς αυξημένου τόνου αυτών και συνεπακόλουθης ακράτειας από κατακράτηση (Granger et al. 2020). Εξαιτίας αυτής, το ζώο εκτίθεται σε κίνδυνο ουρολοιμώξεων του κατώτερου ουροποιητικού, ουρο-ελκών, βλάβης του τοιχώματος της ουροδόχου κύστης λόγω υπερέκτασης, ουροπεριτοναίου και, σε πιο σοβαρές περιπτώσεις, βλάβης και του ανώτερου ουροποιητικού (Sherman & Olby 2004). Είναι εμφανές λοιπόν ότι η δυσλειτουργία της ουροδόχου κύστης μπορεί να υποβαθμίσει την ποιότητα ζωής του ζώου, οπότε αποτελεί μια επιπλέον πρόκληση για τον κηδεμόνα του και πρέπει να αντιμετωπιστεί.
Τα ζώα, λοιπόν, με ΝΒ πρέπει να υφίστανται μηχανική κένωση της ουροδόχου κύστης 3 - 4 φορές την ημέρα (Sherman & Olby 2004). Η κύστη με κατακράτηση που προκύπτει, είναι σκληρή στην ψηλάφηση και η κένωσή της αναμένεται να είναι δύσκολη (Cook et al. 2019). Εναλλακτικά μπορεί να εφαρμοστεί διαλείπων άσηπτος καθετηριασμός της ουρήθρας, αφού μόνιμος καθετηριασμός μπορεί να προκαλέσει δευτερεύουσες επιπλοκές όπως ουρολοιμώξεις και τραυματισμό του τοιχώματος του ουροποιητικού (Sherman & Olby 2004). Κάτι τέτοιο μπορεί να αποτελέσει ούτως ή άλλως παροδική λύση κυρίως σε αρσενικά ζώα, αφού ο καθετηριασμός θηλυκών απαιτεί προχωρημένες δεξιότητες από τον κλινικό (Cook et al. 2019).
Φαρμακευτική αγωγή για να διευκολύνει τη μηχανική κένωση της σπαστικής ουροδόχου κύστης συνήθως απαιτείται στην οξεία φάση της κάκωσης του ΝΜ. Ενδεικτικά παρατίθενται τα παρακάτω φάρμακα:
Α) Διαζεπάμη 0,25 - 0,5 mg kg-1 από το στόμα 20 λεπτά προ κένωσης προκαλεί χάλαση του έξω σφιγκτήρα της ουρήθρας (Sherman & Olby 2004) (Granger et al. 2020)
Β) Φαινοξυβενζαμίνη 0,5 mg kg-1 από το στόμα κάθε 8 - 12 ώρες προκαλεί χάλαση του έσω σφιγκτήρα της ουρήθρας (Sherman & Olby 2004) (Granger et al. 2020)
Γ) Άλλοι α αδρενεργικοί αναστολείς μπορούν επίσης να χρησιμοποιηθούν (πχ πραζοσίνη, αλφουζοσίνη) (Olby et al. 2022) (Granger et al. 2020)
Δεν υπάρχουν μελέτες που να υποστηρίζουν τον συνδυασμό των φαρμάκων αυτών. Φαίνεται επίσης ότι η χρήση τους για διευκόλυνση της μηχανικής κένωσης της κύστης δεν απαιτείται μετά από κάποιες εβδομάδες (Granger et al. 2020). Πιθανή ουρολοίμωξη πρέπει να αντιμετωπιστεί με τα κατάλληλα αντιβιοτικά, μετά από καλλιέργεια και δοκιμή ευαισθησίας (Sherman & Olby 2004). Ο κτηνίατρος υποχρεούται να διαφοροποιήσει την ουρολοίμωξη από την υποκλινική βακτηριουρία, στην οποία η αντιβιοθεραπεία σπάνια απαιτείται (Weese et al. 2019).
Αφόδευση
Όπως και με την ούρηση, η φυσιολογική λειτουργία της αφόδευσης επίσης διαταράσσεται σε τραυματισμό του ΝΜ (Granger et al. 2020).
Στις κακώσεις της ΘΟ μοίρας, το πρόβλημα που προκύπτει είναι ο συνεχής τόνος του έξω σφιγκτήρα του πρωκτού και η συσσώρευση κοπράνων στο έντερο, μέχρις ότου η αυξημένη πίεση και διάταση του απευθυσμένου από αυτά να προκαλέσει αντανακλαστική ακούσια κένωση (Granger et al. 2020). Η πιο πρακτική και αποτελεσματική αντιμετώπιση της ακράτειας κοπράνων είναι δίαιτα υψηλής θρεπτικής αξίας και χαμηλού υπολείμματος (πχ. gastrointestinal diets, υποαλλεργικές δίαιτες), η οποία μειώνει τόσο τον όγκο όσο και την υγρασία των κοπράνων, οπότε το πρόβλημα γίνεται πιο διαχειρίσιμο (Granger et al. 2020). Υπάρχει, ωστόσο, συζήτηση για την ορθότερη περιεκτικότητα του σιτηρεσίου σε φυτικές ίνες. Επιπλέον, η καθιέρωση ενός καθημερινού προγράμματος μπορεί επίσης να φανεί χρήσιμη στην διαχείριση. Μαζί με την κένωση της ουροδόχου κύστης συνήθως επέρχεται και αφόδευση, γεγονός που μπορεί να υποβοηθηθεί από μια ήπια διέγερση του περινέου (Granger et al. 2020). Για κάποιους σκύλους απαιτείται γεύμα ή άσκηση για να μπορέσουν να αφοδεύσουν (Granger et al. 2020). Γενικότερη καθαριότητα και περιποίηση του δέρματος του περινέου είναι απαραίτητη για πρόληψη μολύνσεων και λοιπών δυσμενών καταστάσεων (Granger et al. 2020). Πρέπει να τονιστεί, συνεπώς, ότι πρακτικά δεν επέρχεται ακράτεια κοπράνων και ότι οι αντανακλαστικές κινήσεις του πρωκτικού σφιγκτήρα βοηθούν στην κένωση.
Εκ των προαναφερθέντων, ζώα με ΝΒ είναι δεδομένο ότι θα έχουν προβλήματα ούρησης και αφόδευσης, τα οποία όμως, μπορούν να αντιμετωπιστούν, τουλάχιστον ως ένα βαθμό.
Φυσική αποκατάσταση
Διάφορες τεχνικές έχουν προταθεί που να στοχεύουν στην υποβοήθηση ενός ζώου να αναπτύξει ΝΒ, αλλά δεν είναι σκοπός του άρθρου η αναλυτική αναφορά στην φυσικοθεραπεία.
Παρότι δεν είναι αποδεδειγμένο, υπάρχουν ενδείξεις ότι ένα εντατικό πρόγραμμα αποκατάστασης ίσως ευνοήσει ένα ζώο με απώλεια της ΕΒΑΑ περισσότερο, παρά ένα βασικό πρόγραμμα που περιλαμβάνει μόνο παθητικό εύρος κίνησης και υποβοηθούμενη βάδιση (Lewis et al. 2020, Olby et al. 2022).
Το πρόγραμμα πρέπει να ξεκινήσει εντός 1 ή 2 εβδομάδων από τη βλάβη και να διαρκέσει τουλάχιστον 8 εβδομάδες (Gallucci et al. 2020). Η από νωρίς έναρξη της αποκατάστασης σε ζώα χωρίς ΕΒΑΑ φαίνεται να βελτιώνει τα ποσοστά ανάπτυξης ΝΒ (Olby et al. 2022).
Στην βιβλιογραφία υπάρχουν αναφορές για διάρκεια φυσικοθεραπείας που κυμαίνεται από κάποιες μέρες μέχρι μήνες (Lovely et al. 1985, Gallucci et al. 2017, Gallucci et al. 2020, Martins et al. 2021, Olby et al. 2022). Πάντως, μεγαλύτερη εντατικότητα (δηλαδή περισσότερες μέρες της εβδομάδας, περισσότερες συνεδρίες φυσικοθεραπείας και περισσότερες συνεδρίες υδροθεραπείας σε διάδρομο κάτω από το νερό) συνδέεται με πιο αξιοσημείωτη βελτίωση της νευρολογικής εικόνας και μικρότερο χρόνο προς την επίτευξη βαδίσματος που να φέρει το βάρος του ζώου (weight bearing stepping) (Olby et al. 2022).
Όσον αφορά ειδικότερα σε ζώα που παρέλυσαν μετά από ΠΜΔ τύπου Ι κατά Hansen στην ΘΟ μοίρα, οι αναφερόμενες συχνότητες φυσικοθεραπείας είναι 1 με 3 φορές την ημέρα για ασθενείς που νοσηλεύονται, 1 με 3 φορές την εβδομάδα για ασθενείς που πρόκειται να επισκέπτονται την κλινική ειδικά για την συνεδρία και 1 με 5 φορές την ημέρα για ασθενείς που κάνουν την φυσικοθεραπεία τους στο σπίτι (Olby et al. 2022).
Είναι σημαντικό να σημειωθεί ότι τα πρωτόκολλα πρέπει να είναι σχεδιασμένα για το κάθε περιστατικό ξεχωριστά (Olby et al. 2022). Επίσης πρέπει να είναι δυναμικά και να τροποποιούνται με την πάροδο του χρόνου και την διαπίστωση βελτίωσης ή μη ανταπόκρισης (Olby et al. 2022).
Παρακάτω αναφέρονται τεχνικές που μπορούν να χρησιμοποιηθούν, ταξινομημένες σε φθίνουσα σειρά πρακτικότητας και ευκολίας.
Υποβοηθούμενη ορθοστασία
Η επίδραση που έχει η προσθήκη βάρους στην επανάκτηση της βάδισης είναι ευρέως γνωστή (Lovely et al. 1985, Tillakaratne et al. 2001, Edgerton et al. 2007, See & de Leon, 2012). Έτσι, βασικό μέρος του προγράμματος αποκατάστασης πρέπει να αποτελεί η προσπάθεια το ζώο να μπορεί να στηρίξει το βάρος του (Campbell & Huntingford 2016, Olby et al. 2022).
Άσκηση (Step training)
Έρευνα που αξιολόγησε την ικανότητα βάδισης, μετά από διατομή του ΝΜ, σε γάτες που έκαναν άσκηση σε διάδρομο και σε γάτες που δεν ασκούνταν (De Leon et al. 1998), έδειξε ότι οι πρώτες περπάτησαν σε μεγαλύτερο ποσοστό και καλύτερα από τις τελευταίες.
Η επανεκμάθηση του ζώου να βαδίζει μπορεί να γίνει σε ηλεκτρικό διάδρομο ή/και μέσω υδροθεραπείας.
Tα αισθητικά ερεθίσματα που ασκούνται στο πέλμα παίζουν σημαντικό ρόλο στη φυσιολογία της βάδισης (Lovely et al. 1986, Tillakaratne et al. 2002). H υδροθεραπεία, η οποία καλό είναι να προηγείται της χρήσης χερσαίου διαδρόμου (Spinella et al. 2022) μπορεί να γίνει σε δύο μορφές: βαδίζοντας σε υδροδιάδρομο ή κολυμπώντας (Sherman & Olby 2004).
Εύρος κίνησης (Range of motion, ROM)
Πρόκειται για την τεχνική κατά την οποία η άρθρωση υπόκειται σε παθητική ή ενεργητική κάμψη και έκταση. Έτσι αποφεύγονται οι δυσμενείς επιπτώσεις που θα προέκυπταν από την ακινητοποίησή της, οι οποίες μεταξύ άλλων συμπεριλαμβάνουν οστεοπόρωση, μορφολογικές και βιοχημικές μεταβολές στον αρθρικό χόνδρο, απώλεια της ελαστικότητας των μυών κ.α (Sherman & Olby 2004).
Φαρμακευτική αγωγή
Συνεχώς ερευνάται αν διάφορες φαρμακευτικές ουσίες μπορούν να χρησιμοποιηθούν για να διευκολύνουν τη διέγερση του νωτιαίου μυελού και την απόκρισή του σε αισθητικά ερεθίσματα. Αυτές δρουν μέσω σεροτονινεργικής, νοραδρενεργικής ή γλουταμινεργικής δράσης ή, αντιθέτως, μέσω κινητοποίησης των ανασταλτικών νευροδιαβιβα- στών γλυκίνης και GABA (Edgerton et al. 2008). Ακόμα όμως δεν έχει γίνει χρήση τους στην καθημερινή κλινική πράξη, οπότε δεν θα επεκταθούμε περαιτέρω (Martins et al. 2022).
Εξάσκηση της ιδιοδεκτικής αισθητικότητας
Πρόκειται για ασκήσεις που αποσκοπούν στην αύξηση της ιδιοδεκτικότητας και χρήσης των άκρων από το ζώο. Προϋπόθεση για να εκτελεστούν, είναι να μπορεί το ζώο να φέρει αρκετό από το βάρος του και να μπορεί να περπατά με κάποια βοήθεια (Sherman & Olby 2004).
Ραχιαία διέγερση
Η τοποθέτηση ηλεκτροδίων και η τονική διέγερση της ραχιαίας επιφάνειας της οσφυοϊεράς μοίρας της σπονδυλικής στήλης μπορεί να προκαλέσει κινήσεις σε ζώα με πλήρη διατομή του ΝΜ (Edgerton et al. 2008). Μελέτες σε αρουραίους έδειξαν ότι ο συνδυασμός της μεθόδου αυτής μαζί με φάρμακα έχει συνεργικό αποτέλεσμα στην επίτευξη κίνησης (Edgerton et al. 2008). Άλλες μορφές ηλεκτροδιέγερσης ενσωματωμένες στο πρόγραμμα αποκατάστασης φαίνεται επίσης να βοηθούν στην επανάκτηση της βάδισης, όπως η Interferential Electical Stimulation (IES), Functional Electrical Stimulation (FES), και Transcutaneous Electrical Spinal Cord Stimulation (TESCS) (Martins et al. 2021).
Αποτελεσματικότητα τεχνικών αποκατάστασης
Ενδείξεις βελτίωσης και ανάκτησης ΝΒ στην πορεία της αποκατάστασης είναι η μη ανάγκη διέγερσης του περινεϊκού αντανακλαστικού για να σταθεί/κινηθεί το ζώο, η μη ανάγκη εξωτερικής υποβοήθησης της αρχικής κάμψης των οπισθίων άκρων, η επίτευξη περισσοτέρων βημάτων που φέρουν το βάρος του, η βελτίωση της ποιότητας και διάρκειας του βαδίσματος, η ικανότητα βάδισης σε μεγαλύτερες ταχύτητες του διαδρόμου, η μη ανάγκη εξωτερικής υποστήριξης του βάρους και η ορθότερη τοποθέτηση του πέλματος (Lovely et al. 1985, de Leon et al. 1998, See & de Leon, 2012). Όπως ήδη αναφέρθηκε, ο χρόνος που απαιτείται για την επίτευξη ΝΒ ποικίλλει (Lovely et al. 1985, Gallucci et al. 2017, Gallucci et al. 2020, Martins et al. 2021, Olby et al. 2022), οπότε η παρατήρηση κάποιων από τα προαναφερθέντα κλινικών σημείων βελτίωσης θα πρέπει να προϊδεάζει τον κλινικό για πιθανή θετική έκβαση και να τον προτρέπει στη συνέχιση της προσπάθειας αποκατάστασης.
Σε έρευνα των Gallucci et al. (2017) που συμπεριέλαβε 81 σκύλους χωρίς ΕΒΑΑ, οι οποίοι υποβλήθηκαν σε πρόγραμμα αποκατάστασης, το 59% αυτών ανέπτυξε ΝΒ σε διάστημα κατά μέσο όρο 75 ημερών. Σε μεταγενέστερη έρευνα των Gallucci et al. το 2021, βρέθηκε ότι το 45% των γατών ανέπτυξε ΝΒ με μέσο όρο διάρκειας της αποκατάστασης τις 46 ημέρες (και εύρος 15-302 ημέρες). Φαίνεται λοιπόν ότι περίπου τα μισά ζώα που υποβλήθηκαν σε φυσικοθεραπεία ανέπτυξαν ΝΒ.
Συμπεράσματα
Εν κατακλείδι, σκύλοι και γάτες που υφίστανται οξεία κάκωση στη ΘΟ μοίρα του ΝΜ η οποία προκαλεί απώλεια της ΕΒΑΑ, έχουν πιθανότητα να αναπτύξουν ΝΒ. Αυτό ενώ αποδίδεται στην πλαστικότητα του νευρικού συστήματος, μπορεί να υποβοηθηθεί και από ένα πρόγραμμα φυσικής αποκατάστασης σχεδιασμένο σύμφωνα με τις ανάγκες του κάθε ζώου, που αφενός να προετοιμάσει το μυοσκελετικό σύστημα του ζώου και αφετέρου να συνδράμει στην ανάπτυξη των φυσιολογικών αλλαγών που ευθύνονται για τη ΝΒ. Η ΝΒ προσδίδει προοπτικές όσον αφορά στην περιπατητικότητα του ζώου, ωστόσο δεν πρέπει να αναμένεται και αποκατάσταση φυσιολογικής ούρησης. Εντούτοις, η ακράτεια ούρων και κοπράνων θα μπορούσε να αντιμετωπιστεί από ένα αφοσιωμένο κηδεμόνα, αποφασισμένο να βρεί το σωστό πρόγραμμα που ταιριάζει στο ζώο του.
Σύγκρουση συμφερόντων
Οι συγγραφείς δηλώνουν ότι δεν υπάρχει σύγκρουση συμφερόντων.
Υπεύθυνη αλληλογραφίας:
Αλίκη Γρουτίδου
Αυτή η διεύθυνση ηλεκτρονικού ταχυδρομείου προστατεύεται από τους αυτοματισμούς αποστολέων ανεπιθύμητων μηνυμάτων. Χρειάζεται να ενεργοποιήσετε τη JavaScript για να μπορέσετε να τη δείτε.
Βιβλιογραφία
- Aikawa T, Fujita H, Kanazono S, Shibata M & Yoshigae Y (2012) Longterm neurologic outcome of hemilaminectomy and disk fenestration for treatment of dogs with thoracolumbar intervertebral disk herniation: 831 cases (2000–2007). J Am Vet Med Assoc 241, 1617–1626.
- Añor S (2004) Monoparesis. In: BSAVA Manual of Canine and Feline Neurology. Platt SR & Olby NJ eds. 3rd ed. BSAVA, Gloucester, UK, pp. 265-279.
- Bucher D (2009) Central pattern generators. In: Encyclopedia of Neuroscience. Squire L ed. Elsevier, pp. 691-700.
- Castel A, Olby NJ, Ru H, Mariani CL & Muñana KR, Early PJ (2019) Risk factors associated with progressive myelomalacia in dogs with complete sensorimotor loss following intervertebral disc extrusion: a retrospective case-control study. BMC Vet Res 15, 1–9.
- Castel A, Olby NJ, Ru H, Mariani CL & Muñana KR, Early PJ (2017) Clinical Characteristics of Dogs with Progressive Myelomalacia Following Acute Intervertebral Disc Extrusion. J Vet Intern Med 31, 1782-1789.
- De Lahunta A, Glass E, Kent M (2021) Lower Motor Neuron: General Visceral Efferent System. In: de Lahunta’s Veterinary Neuroanatomy and Clinical Neurology, 5th ed, Saunders Elsevier, Philadelphia, pp. 203-229.
- De Lahunta A, Glass E, Kent M (2021) Upper Motor Neuron. In: de Lahunta’s Veterinary Neuroanatomy and Clinical Neurology, 5th ed, Saunders Elsevier, Philadelphia, pp. 230-245.
- De Leon RD, Hodgson JA, Roy RR, Edgerton VR (1998) Full weight-bearing hindlimb standing following stand training in the adult spinal cat. J Neurophysiol 80(1), 83-91.
- De Leon RD, Hodgson JA, Roy RR & Edgerton VR (1998) Locomotor Capacity Attributable to Step Training Versus Spontaneous Recovery After Spinalization in Adult Cats. J Neurophysiol 79, 1329–1340.
- Edgerton VR, Courtine G, Gerasimenko YP, Lavrov I, Ichiyama RM, Fong AJ, Cai LL, Otoshi CK, Tillakaratne NJ, Burdick JW & Roy RR (2008) Training locomotor networks. Brain Res Rev 57(1), 241254.
- Fitzmaurice S (2010) The neurological examination. In: Small Animal Neurology. Nind F ed. Saunders Elsevier, Edinburgh, pp. 6-34.
- Fitzmaurice S (2010) Gait - an introduction. In: Small Animal Neurology. Nind F ed. Saunders Elsevier, Edinburgh, pp.181-185.
- Gallucci A, Dragone L, Al Kafaji T, Menchetti M, Del Magno S & Gandini G(2021) Outcome in Cats with Acute Onset of Severe Thoracolumbar Spinal Cord Injury Following Physical Rehabilitation. Vet Sci 8(2), 1-11.
- Gallucci A, Dragone L, Menchetti M, Gagliardo T, Pietra M, Cardinali M & Gandini G (2017) Acquisition of Involuntary Spinal Locomotion (Spinal Walking) in Dogs with Irreversible Thoracolumbar Spinal Cord Lesion: 81 Dogs. J Vet Intern Med 31, 492-497.
- Garosi L (2004) The neurological examination. In: BSAVA Manual of Canine and Feline Neurology. Platt SR & Olby NJ eds. 3rd ed. BSAVA, Gloucester, UK, pp. 1-23.
- Granger N, Carwardine D (2014) Acute Spinal Cord Injury Tetraplegia and Paraplegia in Small Animals. Vet Clin Small Anim 44, 1131-1156.
- Granger N, Olby NJ, Nout-Lomas YS & the Canine Spinal Cord Injury Consortium (CANSORT-SCI) (2020) Bladder and Bowel Management in Dogs With Spinal Cord Injury. Front Vet Sci 7, 583342.
- Hu HZ, Jeffery ND & Granger N (2018) Somatosensory and motor evoked potentials in dogs with chronic severe thoracolumbar spinal cord injury. Vet J 237, 49–54.
- Jeffery ND, Barker AK, Hu HZ, Alcott CJ, Kraus KH, Scanlin EM, Granger N & Levine JM (2016) Factors associated with recovery from paraplegia in dogs with loss of pain perception in the pelvic limbs following intervertebral disk herniation. J Am Vet Med Assoc 248, 386–394.
- Jeffery ND, Blakemore WF (1999) Spinal cord injury in small animals 1. Mechanisms of spontaneous recovery. Veterinary Record 144, 407–413.
- Kerwin S, Levine M & Hicks D (2012) Thoracolumbar Spine. In: Veterinary Surgery Small Animal. Tobias K & Johnston S ed. Saunders Elsevier, Canada, pp. 449-475.
- Lewis MJ, Cohen EB & Olby NJ (2018) Magnetic resonance imaging features of dogs with incomplete recovery after acute, severe spinal cord injury. Spinal Cord 56,133–141.
- Lewis MJ, Jeffery ND, Olby NJ & the Canine Spinal Cord Injury Consortium (CANSORT-SCI) (2020) Ambulation in Dogs With Absent Pain Perception After Acute Thoracolumbar Spinal Cord Injury. FrontVet Sci 7, 560.
- Lewis MJ, Laber E & Olby NJ (2019) Predictors of response to 4-aminopyridine in chronic canine spinal cord injury. J Neurotrauma 36, 1428–1434.
- Lewis MJ & Olby NJ (2017) Development of a clinical spasticity scale for evaluation of dogs with chronic thoracolumbar spinal cord injury. Am J Vet Res 78, 854-861.
- Lovely RG, Gregor RJ, Roy RR & Edgerton VR (1986) Effects of training on the recovery of full-weight-bearing stepping in the adult spinal cat. Experimental Neurology 92, 421–435.
- Olby N, da Costa R, Levine J, Stein V & the Canine Spinal Cord Injury Consortium (CANSORT SCI) (2020) Prognostic Factors in Canine Acute Intervertebral Disc Disease. Front Vet Sci 7, 596059.
- Olby N, Harris T, Burr J, Muñana K, Sharp N & Keene B (2004) Recovery of Pelvic Limb Function in Dogs following Acute Intervertebral Disc Herniations. J Neurotrauma 21, 49-59.
- Olby N, Jeffery N (2012) Pathogenesis and Physiology of Central Nervous System Disease and Injury. In: Veterinary Surgery: Small Animal vol 1. Tobias K & Johnston S eds. Elsevier Saunders, Misouri, pp. 374-511.
- Olby NJ, Levine J, Harris T, Muñana K, Skeen T& Sharp N (2003) Long-term functional outcome of dogs with severe injuries of the thoracolumbar spinal cord: 87 cases (1996–2001). J Am Vet Med Assoc 222, 762–769.
- Olby N, Moore S, Brisson B, Fenn J, Flegel T, Kortz G, Lewis M & Tipold A (2022) ACVIM consensus statement on diagnosis and management of acute canine thoracolumbar intervertebral disc extrusion. J Vet Intern Med 36, 1570-1596.
- Rossignol S, Chau C, Brustein E, Belanger M, Barbeau H & Drew T (1996) Locomotor capacities after complete and partial lesions of the spinal cord. Acta Neurobiol Exp 56, 449-463.
- Rossignol S, Drew T, Brustein E & Jiang W (1999) Locomotor performance and adaptation after partial or complete spinal cord lesions in the cat. Progress in Brain Research 123, 349-365.
- Schatzberg S, Kent M & Platt S (2012) Neurological Examination and Neuroanatomin Diagnosis. In: Veterinary Surgery: Small Animal, vol 1.Tobias K & Johnston S eds. Elsevier Saunders, Misouri, pp. 325-340.
- See PA& de Leon RD (2013) Robotic loading during treadmill training enhances locomotor recovery in rats spinally transected as neonates. J Neurophysiol 110, 760-767.
- Sharp N, Wheeler S (2005) Functional Anatomy. In: Small Animal Spinal Disorders: Diagnosis and Surgery. Rodenhuis J ed. 2nd ed. Elsevier Mosby, n.p, pp.1-17.
- Sherman J, Olby NJ (2004) Nursing and rehabilitation of the neurological patient. In: BSAVA Manual of Canine and Feline Neurology. Platt SR & Olby NJ eds. 3rd ed. BSAVA, Gloucester, UK, pp. 394-407.
- Smith JL, Smith LA, Zernicke RF & Hoy M (1982) Locomotion in exercised and nonexercised cats cordotomized at two or twelve weeks of age. Experimental Neurology 76(2), 393-413.
- Tefend Campbell M & Huntingford J (2016) Nursing Care and Rehabilitation Therapy for Patients with Neurologic Disease. In: Practical Guide to Canine and Feline Neurology. Dewey & da Costaeds. 3rd ed, Wiley, Iowa, pp. 559-584.
- Tillakaratne NJ, de Leon RD, Hoang TX, Roy RR, Edgerton VR, Tobin A J (2002) Use-dependent modulation of inhibitory capacity in the feline lumbar spinal cord. J Neurosci 22, 3130-3143.
- Weese J.S, Blondeau J, Boothe D, Guardabassi L.G, Gumley N, Papich M, Jessen L.R, Lappin M, Rankin S, Westropp J.L, Sykes J (2019) International Society for Companion Animal Infectious Diseases (ISCAID) guidelines for the diagnosis and management of bacterial urinary tract infections in dogs and cats, The Veterinary Journal 247, 8-25.