Ελένη Πραστίτη κτηνίατρος, Ζωή Τζενετίδου κτηνίατρος, Χρήστος Κουτίνας κτηνίατρος, PhD, Γεώργιος Καζάκος κτηνίατρος, PhD
Κλινική Ζώων Συντροφιάς, Τμήμα Κτηνιατρικής, Α.Π.Θ., Θεσσαλονίκη
MeSH keywords:
cardiac arrhythmias, cat, dog
Περίληψη
Οι διαταραχές του καρδιακού ρυθμού κατά την περιεγχειρητική περίοδο είναι ένα αρκετά συχνό φαινόμενο. Τόσο ζώα με καρδιακά νοσήματα, όσο και μη καρδιοπαθή ασθενή ή υγιή ζώα που υποβάλλονται σε χειρουργικές επεμβάσεις, είναι δυνατόν να παρουσιάσουν αρρυθμίες κατά την περιαναισθητική περίοδο. Επιπλέον, ορισμένες χειρουργικές παθήσεις, όπως εκείνες του σπλήνα, του κατώτερου ουροποιητικού και το σύνδρομο της διάτασης και στροφής του στομάχου στον σκύλο, συνδέονται σταθερά με την εμφάνιση περιεγχειρητικών αρρυθμιών. Η αναγνώρισή τους και η κατανόηση της προέλευσής τους στηρίζεται στη συνεχή παρακολούθηση των ζωτικών λειτουργιών (monitoring) και επιτυγχάνεται με την εξέταση των βλεννογόνων, την ψηλάφηση του σφυγμού, την μέτρηση της θερμοκρασίας και την χρήση ηλεκτροκαρδιογραφήματος (ΗΚΓ), καπνογράφου, παλμικού οξυμέτρου και την μέτρηση της αρτηριακής πίεσης. Ευρήματα όπως η υπόταση, η δύσπνοια, η συμφόρηση των βλεννογόνων, η υποθερμία, το μειωμένο επίπεδο συνείδησης, η μειωμένη παραγωγή ούρου, η αυξημένη τιμή του γαλακτικού οξέος, που οφείλονται στην παρουσία αρρυθμιών, υποδηλώνουν κακή αιμοδυναμική κατάσταση του ασθενούς και επιβάλλουν την άμεση διόρθωση του υποκείμενου προβλήματος και πολλές φορές την ταυτόχρονη συμπτωματική αντιμετώπιση των προκαλούμενων αρρυθμιών. Επιπλέον, σε περίπτωση που δεν έχουν ακόμα εμφανιστεί συμπτώματα, αλλά στο ΗΚΓ παρατηρούνται ορισμένα «κρίσιμα» χαρακτηριστικά των αρρυθμιών, συστήνεται η χορήγηση κατάλληλων αντιαρρυθμικών φαρμάκων, ώστε να αποτραπεί η εμφάνιση κλινικών εκδηλώσεων σε μετέπειτα χρόνο ή ο ξαφνικός θάνατος του ασθενούς. Το είδος (ταχυαρρυθμίες, βραδυαρρυθμίες) και η περιοχή προέλευσης (υπερκοιλιακές, κοιλιακές) των αρρυθμιών καθορίζουν το αντιαρρυθμικό φάρμακο εκλογής που πρέπει να χορηγείται σε κάθε περίπτωση.
Εισαγωγή
Με τους όρους αρρυθμία ή αλλιώς δυσρυθμία περιγράφονται οι διαταραχές του καρδιακού ρυθμού. Στις αρρυθμίες περιλαμβάνονται οι μεταβολές στην καρδιακή συχνότητα, οι αρρυθμίες που σχετίζονται με τις εκτακτοσυστολές και οι διαταραχές στη μεταβίβαση των ώσεων (Martin 2007).
Οι αρρυθμίες κατά την περιεγχειρητική περίοδο είναι ένα αρκετά συχνό φαινόμενο. Τόσο ζώα με παθήσεις της καρδιάς, όπως για παράδειγμα η εκφυλιστική βαλβιδοπάθεια της μιτροειδούς, όσο και μη καρδιοπαθή ζώα, που είναι ασθενή και χρειάζεται να υποβληθούν σε χειρουργική επέμβαση, ή είναι υγιή και θα υποβληθούν σε μια απλή επέμβαση (π.χ. ωοθυκηστερεκτομή), είναι δυνατόν να παρουσιάσουν αρρυθμίες κατά την περιαναισθητική περίοδο (Oyama 2015). Διάφορες έρευνες διαφωνούν σχετικά με το κατά πόσο οι περιαναισθητικές αρρυθμίες σχετίζονται με αυξημένη νοσηρότητα και θνησιμότητα (Beck 2006, Mackenzie et al. 2010, Wendelburg et al. 2014).
Ωστόσο, σε όλες τις περιπτώσεις κρίνεται αναγκαίο ο κλινικός να είναι γνώστης των φυσιολογικών μεταβολών του καρδιακού ρυθμού σε ένα αναισθητοποιημένο ζώο, να τις ξεχωρίζει από τις παθολογικές και να είναι σε θέση, πραγματοποιώντας τις κατάλληλες ενέργειες, να τις προλαμβάνει ή να τις θεραπεύει, όταν υπάρχει ανάγκη.
Μηχανισμός αρρυθμογένεσης
Οι αρρυθμίες διακρίνονται, ανάλογα με τον τρόπο δημιουργίας τους, σε εκείνες που προκύπτουν από διαταραχές στην παραγωγή της ώσης (αυτοματισμός) ή/και από διαταραχές της αγωγιμότητας. Οι διαταραχές της παραγωγής της ώσης μπορούν να προκαλέσουν τόσο βραδυαρρυθμίες όσο και ταχυαρρυθμίες, ενώ διαταραχές στο σύστημα μεταβίβασης των ώσεων μπορεί να οδηγήσουν σε καθυστέρηση αυτής ή σε πλήρη αποκλεισμό της. Επιπλέον, μπορεί να σχετίζονται με την ύπαρξη εκτοπίας (πρόωρες ή έκτοπες εκπολώσεις) (Schober 2010).
Το ακριβές αίτιο μιας περιεγχειρητικής αρρυθμίας δεν μπορεί εύκολα να εξακριβωθεί σε όλες τις περιπτώσεις, καθώς η αρρυθμογένεση μπορεί να οφείλεται σε πολλούς παράγοντες όπως είναι η φλεγμονή, η σήψη, η υποξία, το οξειδωτικό stress, η ισχαιμία και η ίνωση του μυοκαρδίου (Oyama 2015).
Στον Πίνακα 1 παρουσιάζονται οι συχνότερες αρρυθμίες με βάση το μηχανισμό σχηματισμού τους.
Καρδιοπάθειες
Η αναισθησιολογική διαχείριση ενός ασθενούς με συγγενή ή επίκτητη καρδιοπάθεια, ή/και με εγκατεστημένη συμφορητική καρδιακή ανεπάρκεια είναι δύσκολη και απαιτεί γνώσεις, εμπειρία και καλή προετοιμασία. Το είδος των παρατηρούμενων καρδιακών αρρυθμιών και η παθογένεια τους είναι ανάλογες του τύπου της καρδιοπάθειας. Πριν την πραγματοποίηση οποιασδήποτε χειρουργικής επέμβασης, ο ασθενής θα πρέπει να σταθεροποιείται, ενώ, πριν την εγκατάσταση της αναισθησίας, μεταξύ άλλων, πραγματοποιείται ηλεκτροκαρδιογράφημα (ΗΚΓ) για την διαφοροποίηση των αρρυθμιών που προκαλούνται από τα φάρμακα που χρησιμοποιούνται στο αναισθητικό πρωτόκολλο. Μέχρι το ζώο να ανανήψει πλήρως από την αναισθησία θα πρέπει να παρακολουθείται στενά με ΗΚΓ (Gurney & Bradbrook 2016).
Παρόλο που οι καρδιοπάθειες αποτελούν έναν από τους σημαντικότερους παράγοντες πρόκλησης περιαναισθητικών αρρυθμιών, το άρθρο αυτό εστιάζει στην διάγνωση και αντιμετώπισή τους σε μη καρδιοπαθή ζώα, αφού αποτελούν μεγαλύτερη πρόκληση, καθώς η εμφάνιση τους συχνά δεν αναμένεται από τον κλινικό και συνεπώς υποδιαγιγνώσκονται και δεν αντιμετωπίζονται.
Περιαναισθητική παρακολούθηση ζωτικών λειτουργιών (monitoring)
Κατά την περιαναισθητική περίοδο η αναγνώριση των αρρυθμιών και η απόφαση για χορήγηση αντιαρρυθμικής θεραπείας στηρίζεται στη συνεχή παρακολούθηση των ζωτικών λειτουργιών (monitoring) (Oyama 2015). Οι παράμετροι που κρίνεται απαραίτητο να ελέγχονται διαρκώς είναι:
- Ηλεκτροκαρδιογράφημα: Παρέχει πληροφορίες όχι μόνο για τον ακριβή τύπο της αρρυθμίας και την αρχιτεκτονική δομή της καρδιάς, αλλά πολλές φορές βοηθάει στην εκτίμηση του αιτίου πρόκλησής της (Cornick- Seahorn 2006).
- Καρδιακή συχνότητα: Η χρησιμοποίηση οισοφαγικού στηθοσκοπίου διεγχειρητικά είναι σημαντική αν δεν διατίθεται ΗΚΓ (Cornick-Seahorn 2006). Καρδιακή συχνότητα μεγαλύτερη των 180 min-1 ή μικρότερη των 50 min-1 στον σκύλο και μεγαλύτερη των 220 min-1 ή μικρότερη των 90 min-1 στη γάτα, σχετίζονται με αυξημένο κίνδυνο εμφάνισης κλινικών συμπτωμάτων (Oyama 2015).
- Ποιότητα σφυγμού: Εκτός από τη μέτρηση της καρδιακής συχνότητας και την εκτίμηση του ρυθμού, ψηλαφούνται η μηριαία ή άλλες επιφανειακές αρτηρίες για τη διαπίστωση ελλείμματος σφυγμού και την εκτίμηση του χαρακτήρα του σφυγμού, καθώς οι αρρυθμίες τείνουν να τον μεταβάλλουν ανάλογα με τον τύπο και την σοβαρότητά τους (Bonagura 2008).
- Χρόνος αναπλήρωσης τριχοειδών (ΧΑΤ) και χρωματισμός βλεννογόνων: Φυσιολογικά, οι βλεννογόνοι είναι ροδαλοί και ο ΧΑΤ είναι μικρότερος από 2 sec. Ο ζωηρός ερυθρός χρωματισμός, που συνοδεύεται από μείωση του ΧΑΤ, μπορεί να οφείλεται στην αγγειοδιαστολή που προκαλούν η υπερκαπνία, η σήψη, η υποθερμία και η χορήγηση αναισθητικών φαρμάκων (προποφόλη, εισπνευστικά αναισθητικά), παράγοντες που συμβάλλουν στην εμφάνιση αρρυθμιών (Congdon 2015). H ωχρότητα των βλεννογόνων, που συνοδεύεται από αύξηση του ΧΑΤ, είναι ενδεικτική υπότασης, shock, αναιμίας, υποθερμίας και χορήγησης φαρμάκων, όπως οι α-2 αδρενεργικοί αγωνιστές (περιφερική αγγειοσύσπαση) και κάποια οπιοειδή.
- Μέτρηση της θερμοκρασίας: Η υποθερμία μπορεί να αποτελεί τόσο αιτιολογικό παράγοντα πρόκλησης αρρυθμιών, όσο και κλινικό σύμπτωμα αυτών, ως αποτέλεσμα της διαταραχθείσας αιμοδυναμικής κατάστασης (Haskins 2007, Oyama 2015).
- Αναπνευστική συχνότητα και δύσπνοια: Διενεργείται επισκόπηση του θωρακικού τοιχώματος ή/και του ασκού της αναισθητικής μηχανής για τη μέτρηση της αναπνευστικής συχνότητας, την εκτίμηση του βάθους των αναπνοών και την διαπίστωση δύσπνοιας. Ζώα με αρρυθμία πρέπει να λαμβάνουν οξυγόνο καθ’ όλη την περιεργχειρητική περίοδο. Η ταχύπνοια σε ζώο που εμφανίζει αρρυθμίες μπορεί να υποδηλώνει υποξία, υπερκαπνία και οξέωση (Macintire 2006).
- Αρτηριακή πίεση του αίματος: Η αρτηριακή πίεση παρέχει πληροφορίες για την καρδιακή παροχή, την κατάσταση των περιφερικών αγγείων και συνεπώς για τη διαιμάτωση των ιστών. Η υπόταση κατά την περιαναισθητική περίοδο μπορεί να οφείλεται στη δράση των αναισθητικών φαρμάκων (π.χ. φαινοθειαζίνες, ισοφλουράνιο), στις αρρυθμίες ή στα αντιαρρυθμικά φάρμακα που χορηγήθηκαν για την αντιμετώπιση ταχυαρρυθμιών (Mazzaferro 2001, Macintire 2006, Oyama 2015). Για την ικανοποιητική διαιμάτωση του εγκεφάλου και των νεφρών, απαιτείται ελάχιστη μέση αρτηριακή πίεση 60 mmHg τόσο για τον σκύλο όσο και την γάτα (Duke-Novakovski & Carr 2015).
- Παλμική οξυμετρία: Για την αναγνώριση της υποξαιμίας σε ένα ζώο, θεωρείται χρήσιμη η μέτρηση του κορεσμού της αιμοσφαιρίνης σε Ο2 στο αρτηριακό αίμα (SpO2). Η υποξαιμία σε ένα ζώο που εμφανίζει αρρυθμίες μπορεί να αποτελεί τόσο τον αιτιολογικό παράγοντα εμφάνισής τους (ισχαιμία του μυοκαρδίου), όσο και το αποτέλεσμα αυτών (αιμοδυναμική αποσταθεροποίηση). Ζώα που εισπνέουν ατμοσφαιρικό αέρα, πρέπει να έχουν SpO2 πάνω από 92% ενώ ζώα που εισπνέουν 100% Ο2 πρέπει να έχουν SpO2 πάνω από 98%. Πρέπει να σημειωθεί πως μακροσκοπική κυάνωση των βλεννογόνων παρατηρείται σε τιμές SpO2 μικρότερες του 74%, εφόσον δεν συνυπάρχει μέτριου ή σοβαρού βαθμού αναιμία (Ko et al. 2001, Epstein 2005, Pypendop 2005).
- Kαπνομετρία–καπνογραφία: Για ένα φυσιολογικό καπνογράφημα απαιτείται φυσιολογικός κυτταρικός μεταβολισμός, φυσιολογική κυκλοφορία του αίματος και φυσιολογικός αερισμός των κυψελίδων. Πολλές φορές οι παρατηρούμενες διαταραχές μπορεί να αποτελούν μεταξύ άλλων ένδειξη κακής αιμοδυναμικής κατάστασης (Creedon 2013).
- Παραγωγή ούρου: Σε απουσία νεφρικής νόσου, η παραγωγή ούρου αποτελεί έναν καλό δείκτη της νεφρικής ροής του αίματος και κατ’ επέκταση της καρδιακής παροχής. Φυσιολογικά η παραγωγή ούρου είναι μεγαλύτερη από 1 ml kg-1 h-1 και θα πρέπει να υπολογίζεται συχνά, ως δείκτης επαρκούς αιμάτωσης του νεφρικού ιστού (Creedon 2013).
- Εργαστηριακές εξετάσεις: Σε αυτές περιλαμβάνονται η μέτρηση των αερίων σε δείγμα αρτηριακού αίματος, των ηλεκτρολυτών, του γαλακτικού οξέος και της καρδιακής τροπονίνης-Ι. Οι διαταραχές της οξεοβασικής ισορροπίας και των ηλεκτρολυτών αποτελούν τόσο αιτιολογικό παράγοντα πρόκλησης παροδικών αρρυθμιών, όσο και αποτέλεσμα της αιμοδυναμικής αποσταθεροποίησης ως συνέπειας αυτών (Cohen & Tilley 1979). Οι μετρήσεις του γαλακτικού οξέος και της τροπονίνης-Ι πληροφορούν για την αιμάτωση των ιστών και για τυχόν βλάβη στο μυοκάρδιο, αντίστοιχα (Creedon 2013, Hamacher 2015).
Καλοήθεις αρρυθμίες
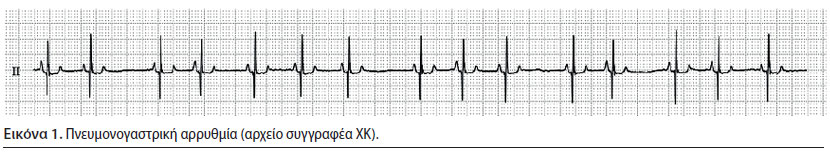
Πνευμονογαστρική αρρυθμία (Εικόνα 1)
Η πνευμονογαστρική αρρυθμία αποτελεί φλεβοκομβικό ρυθμό κατά τον οποίο η συχνότητα των καρδιακών ώσεων αυξάνεται και μειώνεται ισόχρονα (Martin 2007). Συνήθως συνδέεται με την αναπνοή, δηλαδή η συχνότητα αυξάνεται κατά την εισπνοή και μειώνεται κατά την εκπνοή. Επιπλέον, είναι ενδεικτική της παρασυμπαθοτονίας, καθώς σχετίζεται με την αυξημένη δράση του πνευμονογαστρικού νεύρου στον φλεβόκομβο και η ύπαρξή της αποτελεί έναν δείκτη υγείας του μυοκαρδίου, καθώς η συμπαθοτονία συνήθως είναι χαρακτηριστική της καρδιακής ανεπάρκειας (Martin 2007). Παρατηρείται σε υγιείς σκύλους κατά την ανάπαυση, μετά από χορήγηση α-2 αδρενεργικών αγωνιστών και σε σκύλους βραχυκεφαλικών φυλών (Gross 2009, Papich 2016). Πέρα από αυτές τις περιπτώσεις, στις οποίες η πνευμονογαστρική αρρυθμία θεωρείται «καλοήθης», εμφανίζεται και σε ασθενείς σκύλους με αναπνευστικές, νευρολογικές και οφθαλμικές παθήσεις, καθώς και σε ζώα με παθήσεις του στομάχου και του εντέρου. Σε αντίθεση με τον σκύλο, η πνευμονογαστρική αρρυθμία είναι σπάνια στη γάτα και μπορεί να παρατηρηθεί στις ασθένειες που αναφέρθηκαν προηγουμένως, καθώς επίσης και κατά την δύσπνοια ή καρδιακές νόσους. Η πνευμονογαστρική αρρυθμία, αυτή καθ’ αυτή, δεν απαιτεί καμία θεραπεία (Gompf 2011).
Φυσιολογική διακύμανση της καρδιακής συχνότητας
Σε υγιείς οργανισμούς, τόσο στα ζώα όσο και τον άνθρωπο, τα μεσοδιαστήματα R-R του ΗΚΓ δεν είναι σταθερά και μεταβάλλονται ανάλογα με τις φυσιολογικές επιδράσεις που προκύπτουν από τις μεταβολές στην ισορροπία του αυτόνομου νευρικού συστήματος (Spyer 1994). Αυτή η διακύμανση του καρδιακού ρυθμού παρέχει χρήσιμεςπληροφορίες -μεταξύ άλλων- για την κατάσταση του μυοκαρδίου. Συγκεκριμένα, ασθενείς με συμφορητική καρδιακή ανεπάρκεια παρουσιάζουν αυξημένη καρδιακή συχνότητα και μειωμένη διακύμανση του καρδιακού ρυθμού λόγω της χρόνιας ενεργοποίησης του συμπαθητικού συστήματος (Nolan et al. 1992). Συνεπώς, η παρατήρηση σημαντικής διακύμανσης του καρδιακού ρυθμού, υποδηλώνει είτε την ύπαρξη ενός υγιούς μυοκαρδίου, είτε υποκλινική καρδιοπάθεια στην οποία δεν έχει ακόμα εγκατασταθεί συμφορητική καρδιακή ανεπάρκεια (Häggström et al. 1996). Πρέπει να σημειωθεί πως η ακριβής εκτίμηση αυτής της παραμέτρου απαιτεί ειδικό λογισμικό.
Αναγνώριση και θεραπεία αρρυθμιών
Tαχυαρρυθμίες
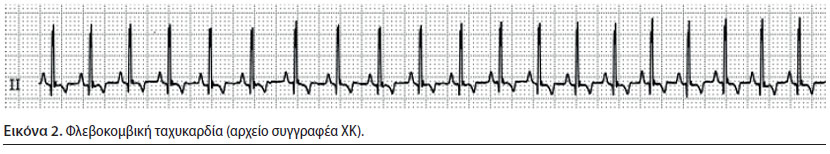
Φλεβοκομβική ταχυκαρδία (Εικόνα 2)
- Ο ρυθμός είναι φλεβοκοβικός αλλά η καρδιακή συχνότητα είναι μεγαλύτερη της φυσιολογικής (πάνω από 140 min-1) (Oyama 2015).
- Κάθε συστολή συνοδεύεται από ψηλαφητό σφυγμό, ενώ όταν η συχνότητα είναι πολύ μεγάλη ο σφυγμός μπορεί να γίνει ασθενής (Oyama 2015).
Η φλεβοκομβική ταχυκαρδία δεν είναι επικίνδυνη αρρυθμία. Εμφανίζεται, συνήθως, μετά από χορήγηση κεταμίνης, ατροπίνης και θειοβαρβιτουρικών ή μετά από έντονη διέγερση του συμπαθητικού συστήματος, όπως συμβαίνει για παράδειγμα στις περιπτώσεις περιεγχειρητικού πόνου, αναιμίας, υποογκαιμίας και μικρού βάθους αναισθησίας (Martin 2007, William 2007). Η αντιμετώπισή της στηρίζεται στην άρση του παράγοντα που την προκάλεσε, δηλαδή στην χορήγηση αναλγητικών φαρμάκων, κατάλληλων υγρών ενδοφλεβίως και την αύξηση του βάθους της αναισθησίας (Cohen 1979, Stepien 2005).
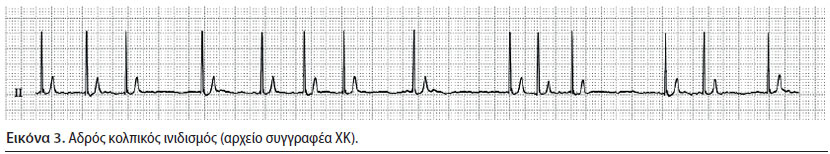
Κολπικός ινιδισμός (Εικόνα 3)
- Το κύμα εκπόλωσης ξεκινά σε τυχαίο χρονικό διάστημα σε περιοχή των κόλπων χωρίς να οδηγεί σε επαρκή σύσπαση τους (Martin 2007).
- Κατά την ακρόαση ο καρδιακός ρυθμός είναι χαοτικός, ενώ κατά την ψηλάφηση του σφυγμού παρατηρείται ένα έλλειμμα της τάξης του 50% σε σχέση με τις καρδιακές ώσεις (Martin 2007).
- Κατά την εξέταση του ΗΚΓ, δεν παρατηρούνται αναγνωρίσιμα επάρματα Ρ, τα συμπλέγματα QRS είναι φυσιολογικά, ενώ το διάστημα R-R είναι χαοτικά ανισόχρονο (Martin 2007).
Ο κολπικός ινιδισμός αποτελεί τη συχνότερη διαγνωσμένη αρρυθμία στα ζώα συντροφιάς και συνήθως προκαλείται λόγω υποκείμενης καρδιακής νόσου και ευθύνεται για τη μείωση της καρδιακής παροχής (Martin 2007). Συνεπώς, η εμφάνιση του κατά την περιαναισθητική περίοδο, συνήθως υποδηλώνει και την ύπαρξή του πριν από την περίοδο αυτήν (Bright 2012). Οι συγγραφείς μετά τη διαπίστωση αυτού του ρυθμού, αφήνουν το ζώο να ανανήψει ακόμα και πρώιμα (εφόσον το στάδιο των χειρισμών το επιτρέπει) και να ελεγχθεί καρδιολογικά πριν αποφασιστεί πως η εμφάνιση αυτής της διαταραχής ήταν παροδική. Ωστόσο, κολπικός ινιδισμός σε ζώα που δεν παρουσίαζαν διαταραχή στη μορφολογία της καρδιάς έχει παρατηρηθεί κατά τη διάρκεια χειρισμών που αυξάνουν τον τόνο του πνευμονογαστρικού νεύρου (π.χ. διασωλήνωση της τραχείας) και αφού προηγουμένως είχαν χορηγηθεί οπιοειδή φάρμακα (βουτορφανόλη, φεντανύλη, μορφίνη) (Moïse et al. 2005). Για την αντιμετώπιση αυτής της οξείας εμφάνισης του κολπικού ινιδισμού, η οποία προκλήθηκε λόγω της διέγερσης του παρασυμπαθητικού συστήματος, έχει χρησιμοποιηθεί επιτυχώς ενδοφλέβια άπαξ (bolus) χορήγηση λιδοκαΐνης (Moïse et al. 2005).
Πρωταρχικός στόχος μετά την διάγνωση του κολπικού ινιδισμού είναι η μείωση της καρδιακής συχνότητας. Συχνότητα πάνω από 180 min-1 (σκύλος) ή 200 min-1 (γάτα) απαιτεί μείωσή της, η οποία επιτυγχάνεται με την ενδοφλέβια χορήγηση αποκλειστών διαύλων ασβεστίου (π.χ. διλτιαζέμη) (Stepien 2005). Συγκεκριμένα, συστήνεται μια ενδοφλέβια άπαξ έγχυση και ακολουθούν επαναληπτικές ενδοφλέβιες εγχύσεις ή συνεχής στάγδην έγχυση (CRI), ώστε ο καρδιακός ρυθμός να διατηρείται εντός των αποδεκτών ορίων για ένα ζώο με κολπικό ινιδισμό, δηλαδή 140-160 min-1 (σκύλος) ή 160-180 min-1 (γάτα) (Stepien 2005, Bright 2012).
Πρώιμες υπερκοιλιακές εκτακτοσυστολές (Εικόνα.4) και υπερκοιλιακή ταχυκαρδία
- Οι πρώιμες υπερκοιλιακές εκτακτοσυστολές (ΠΥΕ) παράγονται από έκτοπη εστία ή εστίες που βρίσκονται σε περιοχή πάνω από τις κοιλίες, οι οποίες εκπολώνονται φυσιολογικά. Μια ομάδα τριών ή περισσότερων ΠΥΕ χαρακτηρίζεται ως υπερκοιλιακή ταχυκαρδία (ΥΤ)(Martin 2007).
- Κάθε εκτακτοσυστολή συνοδεύεται από ασθενή σφυγμό ή απουσία του. Έτσι, στην ΥΤ ο αριθμός των καρδιακών παλμών είναι μεγαλύτερος από τον αριθμό των σφυγμών (Martin 2007).
- Κατά την εξέταση του ΗΚΓ, τα συμπλέγματα QRS εμφανίζονται πρόωρα αλλά έχουν φυσιολογική μορφολογία. Επιπλέον, μπορεί να παρατηρηθούν ή όχι επάρματα P, τα οποία εφόσον είναι αναγνωρίσιμα, είναι συνήθως παθολογικής μορφολογίας. Το διάστημα P-R είναι μικρότερο από αυτό του φλεβοκομβικού ρυθμού.

Όταν οι ΠΥΕ είναι μονήρεις και εμφανίζονται με χαμηλή συχνότητα δεν απαιτούν θεραπεία, διότι δεν συνοδεύονται από μείωση της καρδιακής παροχής. Στις περιπτώσεις αυτές, αρκεί μόνο η άρση του παράγοντα που προκάλεσε την αρρυθμία για την υποχώρησή της (Stepien 2005, Martin 2007). Αντιθέτως, όταν οι ΠΥΕ είναι συχνές ή όταν παρατηρείται έντονου βαθμού ΥΤ -που πολλές φορές μπορεί να φτάσει 400 min-1 (σκύλος), η καρδιακή παροχή ενδέχεται να μειωθεί σημαντικά (Stepien 2005). Στην περίπτωση αυτή, η θεραπεία πέρα από την αντιμετώπιση του υποκειμένου αιτίου επιδιώκει τη μείωση της συχνότητας των ΠΥΕ ή την μετατροπή σε φλεβοκομβικό ρυθμό και την επίτευξη φυσιολογικής καρδιακής συχνότητας, αντίστοιχα (Martin 2007).
Η ενδοφλέβια χορήγηση διλτιαζέμης (Πίνακας 2) αποτελεί το φάρμακο εκλογής, εξαιτίας της ταχείας μείωσης της ανταπόκρισης των κοιλιών στην υπερκοιλιακή ταχυκαρδία και συνεπώς της μείωσης της καρδιακής συχνότητας που προκαλεί (Bright 2012). Επιπλέον, η αρνητική ινοτρόπος δράση που έχει η διλτιαζέμη, είναι μικρότερου βαθμού σε σχέση με αυτή που έχουν άλλα αντιαρρυθμικά φάρμακα που χρησιμοποιούνται στην θεραπεία της ΥΤ, πλεονέκτημα που λαμβάνεται σοβαρά υπόψη σε ζώα υπό γενική αναισθησία, στα οποία τις περισσότερες φορές τα χορηγούμενα αναισθητικά φάρμακα ασκούν αρνητική ινοτρόπο δράση στο μυοκάρδιο (Schwartz 2009).
Σε ζώα σε εγρήγορση, σε συνδυασμό με τη φαρμακευτική αγωγή, συστήνεται η πραγματοποίηση χειρισμών διέγερσης του πνευμονογαστρικού νεύρου, όπως η άσκηση μέτριας πίεσης στους οφθαλμικούς βολβούς και η μάλαξη των καρωτίδων πίσω από τις γωνίες της κάτω γνάθου. Οι χειρισμοί αυτοί μπορεί να τερματίσουν την ΥΤ ή να την επιβραδύνουν, βοηθώντας τον κλινικό να αναγνωρίσει την αρρυθμία (Stepien 2005, Martin 2007). Ωστόσο, η επιστροφή σε φλεβοκομβικό ρυθμό πιθανόν να είναι βραχύβια ή από δύσκολη έως αδύνατη στις περιπτώσεις εκείνες, που εκτός των χειρισμών δεν χορηγούνται ταυτόχρονα αντιαρρυθμικά φάρμακα (Stepien 2005).
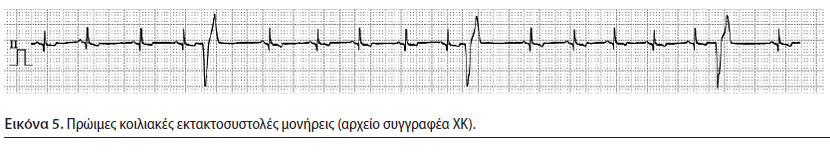
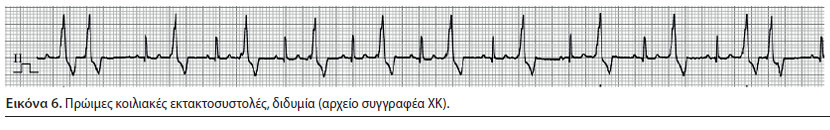
Πρώιμες κοιλιακές εκτακτοσυστολές (Εικόνα 5) και κοιλιακή ταχυκαρδία (Εικόνα 6)
- Οι πρώιμες κοιλιακές εκτακτοσυστολές (ΠΚΕ) παράγονται από έκτοπη εστία ή εστίες που βρίσκονται σε περιοχή των κοιλιών. Στη συνέχεια, η ώση μεταδίδεται από κύτταρο σε κύτταρο, σε κατεύθυνση διαφορετική από την φυσιολογική και όχι μέσω του εξειδικευμένου συστήματος μεταβίβασης των ώσεων. Μια ομάδα τριών ή περισσότερων ΠΚΕ χαρακτηρίζεται ως κοιλιακή ταχυκαρδία (ΚΤ) (Martin 2007).
- Κατά την εξέταση του ΗΚΓ, τα συμπλέγματα QRS έχουν παθολογική και ευρεία μορφολογία και η διάρκειά τους είναι συνήθως πάνω από το 50% των φυσιολογικών. Τα επάρματα Τ είναι συνήθως μεγαλύτερα των φυσιολογικών και αντίθετης κατεύθυνσης από τα QRS των ΠΚΕ, ενώ χαρακτηριστική είναι η απουσία προηγούμενων Ρ επαρμάτων. Όταν μια ΠΚΕ εμφανίζεται πολύ πρώιμα παρατηρείται το φαινόμενο «R-πάνω-στο-T», δηλαδή η ΠΚΕ υπερκαλύπτει το έπαρμα Τ της προηγούμενης συστολής, εξαιτίας του ότι η εκπόλωση των κοιλιών αρχίζει πριν ολοκληρωθεί η αναπόλωση (Martin 2007). Κλινική σημασία έχει και το φαινόμενο εμφάνισης ποικιλόμορφων QRS συμπλεγμάτων που αποτελεί ένδειξη ύπαρξης περισσότερων της μίας έκτοπων εστιών παραγωγής ώσεων (πολυεστιακές) (Martin 2007, Bright 2012). Τόσο η εμφάνιση του φαινομένου «R-πάνω-στο-T» όσο και η παρουσία ποικιλόμορφων QRS συμπλεγμάτων αποτελούν εξαιρετικά σημαντικά ευρήματα διότι μπορεί να οδηγήσουν σε ξαφνικό θάνατο και για αυτό η ανάληψη θεραπείας της αρρυθμίας πρέπει να είναι άμεση (Martin 2007, Bright 2012).
- Η σοβαρότητα της εμφάνισης των ΠΚΕ αξιολογείται με βάση την επίδραση που έχουν στην καρδιακή παροχή. Όταν είναι μονήρεις και σποραδικές, δεν συνοδεύονται από μείωση της καρδιακής παροχής, και επομένως η αναγνώριση και άρση του παράγοντα που προκαλεί την αρρυθμία αρκούν για την αντιμετώπισή της. Όταν όμως η ΚΤ είναι τόσο σοβαρή ώστε να προκαλεί μείωση της καρδιακής παροχής ή όταν παρουσιαστεί το φαινόμενο «R-πάνω-στο-T», κρίνεται απαραίτητη η χορήγηση αντιαρρυθμικών φαρμάκων (Stepien 2005).
Η ενδοφλέβια χορήγηση λιδοκαΐνης (Πίνακας 2) αποτελεί τον ακρογωνιαίο λίθο και το φάρμακο εκλογής για την αντιμετώπιση της οξείας εμφάνισης ΚΤ. Αν η άπαξ χορήγηση λιδοκαΐνης είναι αποτελεσματική, τότε είναι σημαντικό να ξεκινήσει αμέσως και η ενδοφλέβια CRI αυτής. Να σημειωθεί ότι μέχρι να φτάσει η συγκέντρωση λιδοκαΐνης στα επιθυμητά επίπεδα στο αίμα, επιβάλλεται να γίνονται επαναληπτικές εφάπαξ χορηγήσεις. Αν η αρρυθμία εξακολουθεί να υφίσταται κατά την ανάνηψη, στο ζώο μπορούν να χορηγηθούν και αντιαρρυθμικά φάρμακα από το στόμα (π.χ. σοταλόλη). Η χορήγησή τους μπορεί να αρχίσει ενώ το ζώο συνεχίζει να παίρνει την CRI θεραπεία. Στην περίπτωση αυτή, ο ρυθμός χορήγησης της CRI πρέπει να μειώνεται κατά 50% κάθε 6 ώρες (Stepien 2005, Martin 2007).
Οι γάτες μπορεί να εμφανίσουν συμπτώματα τοξίκωσης από λιδοκαΐνη. Συχνότερα εμφανίζονται συμπτώματα από το καρδιαγγειακό (υπόταση, βραδυκαρδία, αρρυθμίες, ασυστολία), πεπτικά συμπτώματα (σιαλόρροια, έμετος) και διαταραχές από το κεντρικό νευρικό σύστημα (αταξία, νυσταγμός, μυϊκός τρόμος, επιληπτικές κρίσεις). Για τον λόγο αυτό, η χρήση της λιδοκαΐνης πρέπει να είναι απόλυτα δικαιολογημένη και να ακολουθείται πάντοτε αυστηρά το δοσολογικό πρωτόκολλο (Martin 2007).

Μετά τις χορηγήσεις των αντιαρρυθμικών φαρμάκων που χρησιμοποιούνται για την αντιμετώπιση των ταχυαρρυθμιών, απαιτείται συστηματικός έλεγχος της μέσης αρτηριακής πίεσης και του καρδιακού ρυθμού. Λόγω της αρνητικής ινοτρόπου και χρονοτρόπου δράσης που έχουν τα φάρμακα αυτά, υπάρχει ο κίνδυνος εμφάνισης υπότασης ή βραδυκαρδίας, ιδιαίτερα στις περιπτώσεις εκείνες που συνυπάρχει ανεπάρκεια του μυοκαρδίου (Bright 2012).
Βραδυαρρυθμίες
Οι περιεγχειρητικές βραδυαρρυθμίες είναι συνήθως παροδικές και σπάνια προκαλούν συμπτώματα που απαιτούν φαρμακευτική παρέμβαση (Bright 2012).
Φλεβοκομβική βραδυαρρυθμία
- Ο ρυθμός είναι φλεβοκομβικός αλλά η καρδιακή συχνότητα είναι μικρότερη της φυσιολογικής (κάτω από 60 min-1 στον σκύλο και κάτω από 90min-1 στη γάτα) (Martin 2007).
- Κάθε συστολή συνοδεύεται από ψηλαφητό σφυγμό (Martin 2007).
- Κατά την εξέταση του ΗΚΓ τα συμπλέγματα P-QRS είναι φυσιολογικά αλλά εμφανίζονται με αργό ρυθμό (Rudloff & Raffe 2012).
Η φλεβοκομβική βραδυκαρδία οφείλεται συχνότερα στη δράση αναισθητικών φαρμάκων όπως οι α-2 αδρενεργικοί αγωνιστές και τα οπιοειδή, και υποχωρεί μετά την πάροδο της δράσης τους ή τη χορήγηση ανταγωνιστών των φαρμάκων αυτών ή ατροπίνης. Στις περιπτώσεις που η φλεβοκομβική βραδυκαρδία οφείλεται σε αίτια όπως οι ηλεκτρολυτικές διαταραχές, ο αυξημένος τόνος του πνευμονογαστρικού νεύρου και η πολύ έντονη υποογκαιμία, η απλή διόρθωση των καταστάσεων αυτών αρκεί για την αποκατάσταση της καρδιακής συχνότητας (Stepien 2005). Σε περίπτωση εμμένουσας ή επικίνδυνης βραδυκαρδίας, δηλαδή, κάτω από 50 min-1 στον σκύλο και κάτω από 90 min-1 στην γάτα, ή όταν εμφανιστούν συμπτώματα μειωμένης καρδιακής παροχής, κρίνεται απαραίτητη η χορήγηση ατροπίνης ενδοφλεβίως (Πίνακας 2). Στο σημείο αυτό, αξίζει να σημειωθεί πως η χορήγηση ατροπίνης για την αντιμετώπιση της βραδυαρρυθμίας που προκαλείται από τους α-2 αδρενεργικούς αγωνιστές αντενδείκνυται, καθώς αυξάνει σημαντικά το έργο και τις απαιτήσεις του μυοκαρδίου σε οξυγόνο και προκαλεί έντονου βαθμού υπέρταση (τιμές μέσης αρτηριακής πίεσης μέχρι 210 mmHg) (Ko 2001). Η επιλογή των α-2 αδρενεργικών αγωνιστών γίνεται συνήθως μόνο σε υγιή ζώα διότι προκαλείται βραδυκαρδία και συνακόλουθη μείωση της καρδιακής παροχής. Η βραδυκαρδία αυτή τις περισσότερες φορές δεν χρήζει αντιμετώπισης. Εφόσον όμως γίνεται πολύ έντονη, οι συγγραφείς προτείνουν τον μερικό ή πλήρη ανταγωνισμό του α-2 αδρενεργικού αγωνιστή με ατιπαμεζόλη, εκτός των άλλων υποστηρικτικών μέτρων που κατά κανόνα λαμβάνονται (υγρά, οξυγόνο). Στην περίπτωση του μερικού ανταγωνισμού η αναισθησία διατηρείται.
Κολποκοιλιακός αποκλεισμός
Πρόκειται για αδυναμία μετάδοσης του κύματος της εκπόλωσης μέσω του κολποκοιλιακού κόμβου και διακρίνεται σε μερικό (πρώτου ή δευτέρου βαθμού) και σε πλήρη (τρίτου βαθμού) αποκλεισμό (Martin 2007).
1) Πρώτου βαθμού κολποκοιλιακός αποκλεισμός
- Παρατηρείται όταν υπάρχει καθυστέρηση στην μετάδοση των ώσεων μέσω του κολποκοιλιακού κόμβου και συνήθως συνοδεύεται από φλεβοκομβικό ρυθμό (Martin 2007).
Η καρδιακή συχνότητα και ο ρυθμός είναι σε φυσιολογικά πλαίσια και επομένως δεν διαπιστώνεται καμία παθολογική μεταβολή κατά την ακρόαση και την ψηλάφηση του σφυγμού (Martin 2007, Rudloff & Raffe 2012). - Κατά την εξέταση του ΗΚΓ, τα συμπλέγματα P-QRS είναι φυσιολογικά αλλά το διάστημα P-R έχει μεγαλύτερη διάρκεια του φυσιολογικού (Brockman et al. 1995).
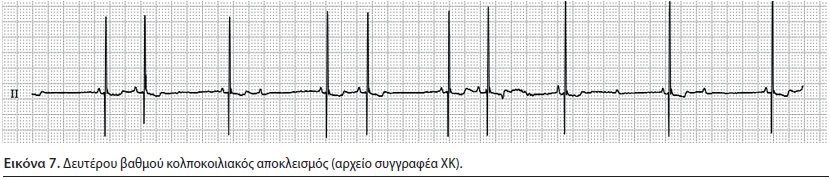
2) Δευτέρου βαθμού κολποκοιλιακός αποκλεισμός (Εικόνα 7)
- Παρατηρείται όταν η μετάδοση της ώσης μέσω του κολποκοιλιακού κόμβου είναι διαλείπουσα, δηλαδή υπάρχουν κολπικές εκπολώσεις που δεν συνοδεύονται από αντίστοιχες των κοιλιών (Martin 2007).
- Κατά την ακρόαση, η σύσπαση των κόλπων μπορεί να γίνει αντιληπτή σαν αμυδρός ήχος κατά την διάρκεια της εκπόλωσής τους (Martin 2007).
- Κατά την εξέταση του ΗΚΓ, παρατηρούνται επάρματα Ρ που δεν συνοδεύονται πάντα από QRS συμπλέγματα. Συνήθως, υπάρχουν δύο επάρματα Ρ για κάθε σύμπλεγμα QRS, αλλά σε προχωρημένο ή σε μεγάλου βαθμού κολποκοιλιακό αποκλεισμό, υπάρχουν περισσότερα επάρματα Ρ πριν την εμφάνιση των κανονικών P-QRS (Tilley & Smith 2016).
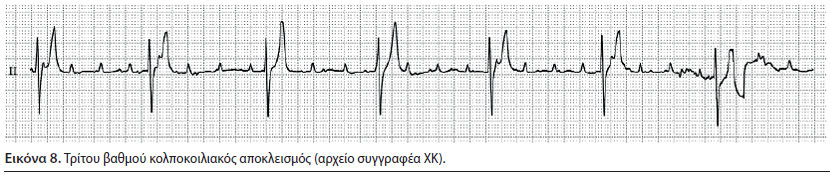
3) Τρίτου βαθμού κολποκοιλιακός αποκλεισμός (Εικόνα 8)
- Παρατηρείται σε πλήρη αδυναμία μετάδοσης του κύματος εκπόλωσης μέσω του κολποκοιλιακού κόμβου, οπότε οι κόλποι και οι κοιλίες συσπώνται ανεξάρτητα. Η συχνότητα των κόλπων είναι μεγαλύτερη από αυτήν των κοιλιών. Τον έλεγχο των κοιλιών αναλαμβάνει ένας άλλος βηματοδότης που βρίσκεται κάτω από τον αποκλεισμό και μπορεί να προέρχεται είτε από το κατώτερο τμήμα του κολποκοιλιακού κόμβου ή από τα σκέλη, είτε από τις ίνες του Purkinje. Στην πρώτη περίπτωση, η μορφολογία του συμπλέγματος QRS θα είναι φυσιολογική (κομβικές εκτακτοσυστολές διαφυγής) με συχνότητα 60-70 min-1, ενώ στην δεύτερη περίπτωση, η μορφολογία των QRS-T θα είναι παράδοξη (κοιλιακές εκτακτοσυστολές διαφυγής) με συχνότητα 30-40 min-1(ιδιοκοιλιακός ρυθμός) (Martin 2007, Tilley & Smith 2016).
- Κατά την ακρόαση παρατηρείται έντονη βραδυκαρδία με καλής ποιότητας σφυγμό και η σύσπαση των κόλπων γίνεται αντιληπτή ως ένας ανεπαίσθητος ήχος που έχει μεγαλύτερη συχνότητα και δεν συνδέεται με τους φυσιολογικούς ήχους S1 και S2 της συστολής και διαστολής των κοιλιών (Martin 2007).
- Κατά την εξέταση του ΗΚΓ δεν διαπιστώνεται συσχετισμός μεταξύ των επαρμάτων P και QRS, ενώ τα επάρματα P εμφανίζονται συχνότερα από τα συμπλέγματα QRS (Martin 2007).
H εμφάνιση πρώτου και δεύτερου βαθμού κολποκοιλιακού αποκλεισμού κατά την αναισθητική περίοδο συνδέεται με την χορήγηση οποιοειδών και α-2 αδρενεργικών αγωνιστών (π.χ. ξυλαζίνη, δεξμεδετομιδίνη) (William 2007). Στις περιπτώσεις αυτές και εφόσον η μέση αρτηριακή πίεση διατηρείται πάνω από 60 mmHg, η ανάληψη θεραπείας δεν είναι απαραίτητη (Smith 2002). Φαρμακευτική θεραπεία αναλαμβάνεται σε περιστατικά με συμπτώματα μειωμένης καρδιακής παροχής, δευτέρου βαθμού κολποκοιλιακό αποκλεισμό με καρδιακή συχνότητα μικρότερη από 40 min-1 στον σκύλο και μικρότερη από 60 min-1 στην γάτα, και σε τρίτου βαθμού κολποκοιλιακό αποκλεισμό. Η θεραπεία συνίσταται κυρίως στην ενδοφλέβια χορήγηση ατροπίνης (Πίνακας 2) (Martin 2007).
Κριτήρια θεραπευτικής παρέμβασης
Η αιμοδυναμική επιβάρυνση του ασθενούς που αποδίδεται στην παρουσία αρρυθμιών, επιβάλλει τη χορήγηση των κατάλληλων αντιαρρυθμικών φαρμάκων ταυτόχρονα με τα υποστηρικτικά μέτρα του καρδιαγγειακού. Επιπλέον, σε περίπτωση που δεν έχουν ακόμα εμφανιστεί συμπτώματα, αλλά στο ΗΚΓ παρατηρούνται ορισμένα «κρίσιμα» χαρακτηριστικά των αρρυθμιών, πάλι κρίνεται απαραίτητη η χορήγηση αντιαρρυθμικών φαρμάκων, ώστε να αποτραπεί η εμφάνιση κλινικών εκδηλώσεων σε μετέπειτα χρόνο ή ο ξαφνικός θάνατος του ασθενούς.
Συμπτώματα αιμοδυναμικής αποσταθεροποίησης (Schwartz 2009, Oyama 2015):
- Υπόταση
- Δύσπνοια
- Συμφόρηση ή αποχρωματισμός των βλεννογόνων
- Ανεπαρκής αιμάτωση των ιστών (μειωμένο επίπεδο συνείδησης, μειωμένη παραγωγή ούρου, αυξημένη τιμή γαλακτικού οξέος)
- Υποθερμία
Κρίσιμα σημεία στο ΗΚΓ:
- Διάρκεια αρρυθμιών μεγαλύτερη από 30 sec (Oyama 2015).
- Κολπικός ινιδισμός με κοιλιακό ρυθμό πάνω από 180 min-1 (σκύλος) ή πάνω από 200 min-1 (γάτα) (Stepien 2005).
- Εμμένουσα καρδιακή συχνότητα πάνω από 180 min-1 ή κάτω από 50 min-1 στον σκύλο και πάνω από 220 min-1 ή κάτω από 90 min-1 στη γάτα (Oyama 2015).
- Συχνές ΠΥΕ (περισσότερες από 30 min-1) ή έντονου βαθμού YT (Stepien 2005).
- ΠΚΕ σε δυάδες ή τριάδες, συχνές, ποικιλόμορφες, εμφάνιση φαινομένου R-πάνω-στο-Τ, γρήγορη ή παρατεταμένη ΚΤ πάνω από 200 min-1 (Stepien 2005, Martin 2007, Schwartz 2009, Oyama 2015).
Στον Πίνακα 2 γίνεται αναφορά στα φάρμακα πρώτης γραμμής και την ακριβή δοσολογία αυτών, που χρησιμοποιούνται στην αντιμετώπιση των περιεγχειρητικών αρρυθμιών.
Νοσήματα που σχετίζονται με περιεγχειρητικές αρρυθμίες
Όπως προαναφέρθηκε, οι περιεγχειρητικές αρρυθμίες εμφανίζονται ως συνέπεια παροδικών και αναστρέψιμων παθολογικών καταστάσεων που συνήθως παρουσιάζονται κατά την περιεγχειρητική περίοδο. Η σοβαρότητα των παροδικών αρρυθμιών ποικίλλει και μπορεί να κυμαίνεται από μια «αθώα» φλεβοκομβική βραδυκαρδία μέχρι μια επικίνδυνη κοιλιακή ταχυκαρδία. Τις περισσότερες φορές, η αντιμετώπιση σε αρχόμενο στάδιο απλά και μόνο του προδιαθεσιακού παράγοντα, αρκεί για την εξαφάνιση των αρρυθμιών (Oyama 2015).
Στον Πίνακα 3 παρουσιάζονται: 1) παραδείγματα παθολογικών καταστάσεων που εμφανίζονται περιαναισθητικά και στις οποίες αναμένονται παροδικές αρρυθμίες, 2) η παθογένεια των αρρυθμιών και 3) το είδος των αρρυθμιών.
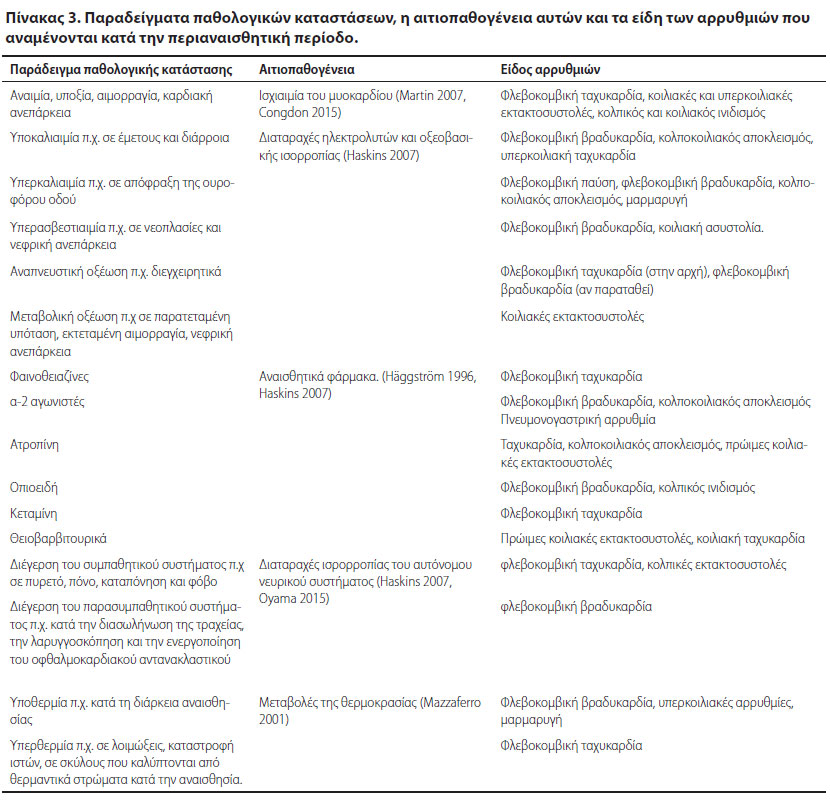
Ορισμένες χειρουργικές παθήσεις, όπως εκείνες του σπλήνα, του κατώτερου ουροποιητικού και το σύνδρομο της διάτασης και στροφής του στομάχου στον σκύλο, συνδέονται σταθερά με την εμφάνιση περιεγχειρητικών αρρυθμιών και ο κλινικός πρέπει να είναι προετοιμασμένος να τις αντιμετωπίσει πριν, κατά τη διάρκεια και μετά τη χειρουργική επέμβαση.
Γαστρική διάταση με ή χωρίς στροφή
Σε ασθενείς με γαστρική διάταση με ή χωρίς στροφή στομάχου, οι κοιλιακές αρρυθμίες κατά την περιαναισθητική περίοδο εμφανίζονται στο 40-50% των περιστατικών (Brockman et al. 1995, Roux 2012). Συγκεκριμένα, η εμφάνιση των αρρυθμιών αναμένεται εντός 12-72 ωρών από την στιγμή της έναρξης των συμπτωμάτων, γεγονός που καθιστά απαραίτητη την συνεχή παρακολούθηση του ΗΚΓ του ασθενούς καθ’ όλη την διάρκεια νοσηλείας του (Roux 2012). Η ισχαιμία του μυοκαρδίου, η διαταραχή της οξεοβασικής ισορροπίας, οι ηλεκτρολυτικές διαταραχές, ο αυξημένος τόνος του συμπαθητικού συστήματος, το σύνδρομο επαναιμάτωσης των ιστών και η απελευθέρωση του κατασταλτικού παράγοντα του μυοκαρδίου από το πάγκρεας, αποτελούν μερικά από τα αίτια πρόκλησης των αρρυθμιών και ταυτόχρονα παράγοντες επιδείνωσής τους (Roux 2012). Παρόλο που έχει διαπιστωθεί πως η εμφάνιση καρδιακών αρρυθμιών μαζί με τη διενέργεια σπληνεκτομής, γαστρεκτομής ή την ύπαρξη νέκρωσης του στομάχου αποτελεί αρνητικό προγνωστικό παράγοντα στην εξέλιξη των περιστατικών, άλλοι ερευνητές φαίνεται να υποστηρίζουν πως η διαπίστωση αρρυθμιών δεν επηρεάζει το ποσοστό θνησιμότητας (Brockman et al. 1995, Brourman et al. 1996). Στις περιπτώσεις που παρατηρούνται επικίνδυνες αρρυθμίες και συμπτώματα αιμοδυναμικής αποσταθεροποίησης που οφείλονται σε αυτές, χορηγείται η κατάλληλη αντιαρρυθμική αγωγή υπό την χορήγηση οξυγόνου και αφού προηγουμένως αναταχθούν η οξεοβασική ισορροπία και οι ηλεκτρολυτικές διαταραχές (Roux 2012). Ιδιαίτερο ενδιαφέρον παρουσιάζει μία έρευνα στην οποία σε ζώα με γαστρική διάταση και στροφή χορηγήθηκε προληπτικά λιδοκαΐνη ενδοφλεβίως άπαξ πριν από την αποσυμπίεση του στομάχου και την ενδοφλέβια χορήγηση υγρών, ακολουθούμενη από λιδοκαΐνη CRI για το πρώτο εικοσιτετράωρο. Η προληπτική χορήγηση λιδοκαΐνης στα ζώα αυτά μείωσε σημαντικά το ποσοστό εμφάνισης περιεγχειρητικών αρρυθμιών, την οξεία νεφρική βλάβη και τον χρόνο μετεγχειρητικής νοσηλείας (Bruchim et al. 2012).
Σπληνεκτομή
Ασθενείς που υποβάλλονται σε σπληνεκτομή λόγω νεοπλασίας, στροφής του σπλήνα ή ανοσοεξαρτώμενων αιματολογικών διαταραχών (π.χ. θρομβοκυτταροπενία, αιμολυτική αναιμία) παρουσιάζουν συχνά κοιλιακές αρρυθμίες (Keyes et al. 1993). Οι αρρυθμίες αυτές οφείλονται στην απελευθέρωση στην συστηματική κυκλοφορία εμβόλων και ελεύθερων ριζών οξυγόνου κατά την διάρκεια χειρισμών του σπλήνα, την αρτηριακή υπόταση, την αναιμία και την δράση άλλων κατασταλτικών παραγόντων στο μυοκάρδιο (Keyes et al. 1993, Marino et al. 1994). Αν και μπορεί να εμφανιστούν κατά τη διάρκεια της περιαναισθητικής περιόδου, αναμένονται συχνότερα διεγχειρητικά ή/και 5-12 ώρες μετά τη χειρουργική επέμβαση και επομένως κρίνεται απαραίτητη η συνεχής παρακολούθηση του ζώου με ΗΚΓ καθ’ όλη τη διάρκεια της νοσηλείας του (Keyes et al. 1993, Marino et al. 1994). Οι αρρυθμίες που παρουσιάζονται σε περιστατικά σπληνεκτομής, σπάνια προκαλούν αιμοδυναμική αποσταθεροποίηση και δεν σχετίζονται με αυξημένα ποσοστά θνησιμότητας. Συνήθως, υποχωρούν εντός 2-5 ημερών μετά την επέμβαση, με την απλή χορήγηση οξυγόνου ή/και μετάγγισης αίματος, και τη διόρθωση της υπότασης και των μεταβολικών διαταραχών. Ωστόσο, εάν εμφανιστούν σοβαρές αρρυθμίες και συμπτώματα αιμοδυναμικής αποσταθεροποίησης που οφείλονται σε αυτές, χορηγείται η κατάλληλη αντιαρρυθμική αγωγή (Moïse et al. 2005).
Σήψη
Παθήσεις που προδιαθέτουν σε σήψη, όπως η πυομήτρα, η ρήξη του εντέρου, τα αποστήματα, κ.ά. είναι πολύ συχνές στην κτηνιατρική πράξη (Laforcade 2010). Η σήψη -ανεξαρτήτως αιτιολογίας- μπορεί να προκαλέσει φλεβοκομβική ή κοιλιακή ταχυκαρδία, πρόωρες κοιλιακές εκτακτοσυστολές και μειωμένη συσταλτικότητα του μυοκαρδίου, που σε συνδυασμό με τον ανεπαρκή κυκλοφορούντα όγκο αίματος πριν τη σταθεροποίηση του ζώου, και συνεπώς το χαμηλό προφορτίο, οδηγούν σε μειωμένη καρδιακή παροχή (Silverstein 2006, Schwartz 2009). Σε ασθενείς με σήψη η θεραπεία αποσκοπεί στην πρόληψη του σηπτικού shock και περιλαμβάνει τη χορήγηση οξυγόνου, τη χορήγηση υγρών ενδοφλεβίως, τη διόρθωση των μεταβολικών και ηλεκτρολυτικών διαταραχών και την εφαρμογή αποτελεσματικής αναλγησίας (Laforcade 2010). Στην περίπτωση εμφάνισης πρόωρων κοιλιακών εκτακτοσυστολών και παρατεταμένων κοιλιακών ταχυαρρυθμιών χορηγούνται τα κατάλληλα αντιαρρυθμικά φάρμακα (Πίνακας 2) (Silverstein 2006, Schwartz 2009). Πολλές φορές, σε ζώα που βρίσκονται σε σηπτικό shock απαιτείται η χορήγηση και αγγειοσυσπαστικών (δοπαμίνη) ή/και θετικών ινοτρόπων (δοβουταμίνη) φαρμάκων (Silverstein 2006, Laforcade 2010).
Υπερκαλιαιμία
Η αναλογία της ενδοκυτταρικής προς την εξωκυτταρική συγκέντρωση του καλίου επηρεάζει την ηλεκτρική δραστηριότητα των μυών (σκελετικών και καρδιακού). Έτσι σε υπερκαλιαιμία, μπορεί να εμφανιστούν βραδυκαρδία ή φλεβοκομβική παύση λόγω της παρατεταμένης εκπόλωσης και αναπόλωσης του συστήματος αγωγής των ώσεων. Περιεγχειρητικά, η υπερκαλιαιμία παρατηρείται στις περιπτώσεις μειωμένης απομάκρυνσης των ούρων (αποφρακτικές νόσοι της ουροφόρου οδού, ολιγουρική νεφρική ανεπάρκεια, ρήξη στο ουροποιητικό σύστημα) αλλά και σε καταστάσεις όπως σακχαρώδης διαβήτης και εκτεταμένες κακώσεις των μαλακών ιστών (Riordan & Schaer 2009). Στο τυπικό ΗΚΓ παρατηρείται βραδυκαρδία, μικρά ή απόντα επάρματα Ρ και αύξηση του ύψους του επάρματος Τ. Ενίοτε στις προκαλούμενες δυσρυθμίες προστίθενται η φλεβοκομβική ταχυκαρδία, η κοιλιακή ταχυκαρδία και ο δευτέρου βαθμού κολποκοιλιακός αποκλεισμός (Tag & Day 2008). Τα ευρήματα του ΗΚΓ δεν σχετίζονται άμεσα με την συγκέντρωση του καλίου στο αίμα, καθώς επηρεάζονται περισσότερο από τον ρυθμό αύξησης ή μείωσης των συγκεντρώσεων του. Η θεραπεία των προκαλούμενων αρρυθμιών στοχεύει στην άρση της υπερκαλιαιμίας, ποικίλει ανάλογα με την συγκέντρωση του καλίου στο αίμα και στηρίζεται στην ενδοκυτταρική μετακίνησή του (Riordan & Schaer 2009). Αξίζει να σημειωθεί πως η αντιμετώπιση της υπερκαλιαιμίας πρέπει να προηγείται της χορήγησης γενικής αναισθησίας.
Υπερθυρεοειδισμός
Έρευνες έχουν καταδείξει πως το 60% των γατών με υπερθυρεοειδισμό που δεν λάμβαναν καμία θεραπεία για αυτόν, εμφάνιζαν συνηθέστερα έντονου βαθμού ταχυκαρδία (πάνω από 240 min-1). Σε μια άλλη έρευνα, το 10% των γατών που υποβλήθηκαν σε θυρεοειδεκτομή εμφάνισαν κοιλιακές και κολπικές δυσρυθμίες κατά την διάρκεια της χειρουργικής επέμβασης (Tag & Day 2008). Οι ηλεκτροκαρδιογραφικές αλλαγές που οφείλονται στην θυρεοτοξίκωση σχετίζονται με την αυξημένη δραστηριότητα του συμπαθητικού νευρικού συστήματος και τις διεγερτικές επιδράσεις των ορμονών του θυρεοειδούς στο μυοκάρδιο (Birchard et al. 1984). Σε κάθε περίπτωση που μία γάτα με υπερθυρεοειδισμό πρέπει να υποβληθεί σε οποιαδήποτε χειρουργική επέμβαση, κρίνεται απαραίτητο ο ασθενής να έχει προηγουμένως γίνει ευθυρεοειδικός και να έχει αποκατασταθεί η καρδιακή συχνότητα, με στόχο να μειωθούν οι πιθανότητες εμφάνισης περιαναισθητικών αρρυθμιών (Peterson et al. 1992, Bond et al. 1988). Η διεγχειρητική διέγερση του συμπαθητικού συστήματος περιορίζεται με την εφαρμογή καλής αναλγησίας και του κατάλληλου αναισθητικού πρωτοκόλλου (Casamian 2009).
Συμπεράσματα
Οι διαταραχές στον καρδιακό ρυθμό κατά την περιαναισθητική περίοδο πρέπει να αναμένονται από τον κλινικό όχι μόνο σε καρδιοπαθή ζώα ή ζώα που υποβάλλονται σε συγκεκριμένες χειρουργικές επεμβάσεις που συνδέονται σταθερά με την εμφάνιση τους, αλλά και σε μη καρδιοπαθή ζώα τα οποία θα υποβληθούν για οποιαδήποτε λόγο σε μια χειρουργική επέμβαση. Το συνεχές monitoring αποτελεί τον ακρογωνιαίο λίθο στην αναγνώριση των κρίσιμων σημείων στο ΗΚΓ και την εντόπιση κλινικών εκδηλώσεων αιμοδυναμικής αποσταθεροποίησης, τα οποία καθιστούν απαραίτητη την χορήγηση της κατάλληλης υποστηρικτικής και αντιαρρυθμικής φαρμακευτικής αγωγής.
Σύγκρουση συμφερόντων
Οι συγγραφείς δηλώνουν ότι δεν υπάρχει σύγκρουση συμφερόντων.
Βιβλιογραφία
- Beck SP (2006) Risk factors associated with short-term outcome and development of perioperative complications in dogs undergoing surgery because of gastric dilatation-volvulus: 166 cases (1992- 2003). J Am Vet Med Assoc 229, 1934-1939.
- Birchard SJ, Peterson ME, Jacobson A (1984) Surgical treatment of feline hyperthyroidism: results of 85 cases. J Am Anim Hosp Assoc 20, 705-709.
- Bonagura JD (2008) Cardiopulmonary System. In: S. J. Βirchard, R. G. Sherding, eds. Saunders manual of small animal practice. 3rd edn. Saunders Elsevier, St Louis, pp. 1421-1731.
- Bond BR, Fox PR, Peterson ME, Skavaril RV (1988) Echocardiographic findings in 103 cats with hyperthyroidism. J Am Vet Med Assoc 192, 1546-1549.
- Bright JM (2012) Perioperative Cardiac Arrhythmias. In: M. J. Bojrad, E. Monnet. Mechanisms of Disease in Small Animal Surgery. 3rd edn. Teton NewMedia, Wyoming, pp. 1-11.
- Brockman DJ, Washabau RJ, Drobatz KJ (1995) Canine gastric dilatation/volvulus syndrome in a veterinary critical care unit: 295 cases (1986-1992). J Am Vet Med Assoc 207, 460-464.
- Brourman JD, Schertel ER, Allen DA, Birchard SJ (1996) Factors associated with perioperative mortality in dogs with surgically managed gastric dilatation-volvulus: 137 cases (1988-1993). J Am Vet Med Assoc 208, 1855-1858.
- Bruchim Υ, Itay S, Shira BH, Kelmer E, Sigal Y, Itamar A, Gilad S (2012) Evaluation of lidocaine treatment on frequency of cardiac arrhythmias, acute kidney injury, and hospitalization time in dogs with gastric dilatation volvulus. J Vet Emerg Crit Care 22, 419-427.
- Casamian D (2009) Cardiovascular effects of systemic or endocrine diseases. In: Proceeding of the SEVC Southern European Veterinary Conference & Congreso Nacional. Barcelona, Spain.
- Cohen RB, Tilley LP (1979) Cardiac Attythmias in the Anesthetized Patient. Vet Clin North Am Small Anim Pract 9, 155-167.
- Congdon JM (2015) Cardioavascular disease. In: L. B. C. Snyder, R. A. Johnson. Canine and Feline Anesthesia and Co-Existing Disease. Willey Blackwell, Wisconsin, pp. 1-54.
- Cornick-Seahorn J (2006) Monitoring critical care patients. In: Proceedings of the North American Veterinary Conference. Orlando, Florida, pp. 79-81.
- Creedon BJM (2013) Assessment and monitoring of blood volume and tissue perfusion. In: Proceedings of the Southern European Veterinary Conference and Congreso Nacional AVEPA. Barcelona, Spain.
- Duke-Novakovski T, Carr A (2015) Perioperative Blood Pressure Control and Management. Vet Clin North Am Small Anim Pract 45, 965-981.
- Epstein S (2017) Pulse oximetry. In: S. J. Ettinger, E. C. Feldman, E. Cote. Textbook of Veterinary Internal Medicine. 8th edn. Elsevier, Toronto, pp. 374-376.
- French A (2008) Arrhythmias: recognition and treatment. In: Proceedings of the 33rd World Small Animal Veterinary Congress. Dublin, Ireland, pp. 119-121.
- Gompf R (2011) Sinus arrhythmia. In: R. V. Morgan. Small animal practise client handouts. 2nd edn. Saunders Elsevier, Maryland Heights, p. 59.
- Gross DR (2009) Cardiovascular Effects of Anesthetics, Sedatives Postoperative Analgesic Agents, and Other Pharmaceuticals. In: D. R. Gross. Animal Models in Cardiovascular Research. 3rd edn. Springer-Verlag, New York, pp. 131-203.
- Gurney M, Bradbrook C (2016) Common ECG abnormalities in the perioperative period. In Practice 38, 219-28.
- Häggström J, Hamlin RL, Hansson K, Kvart C (1996) Heart rate variability in relation to severity of mitral regurgitation in Cavalier King Charles spaniels. J Small Anim Pract 37, 69-75.
- Hamacher L, Deorfelt R, Meuller M, Wess G (2015) Serum Cardiac Troponin I Concentrations in Dogs with Systemic Inflammatory Response Syndrome. J Vet Intern Med 29, 164-170.
- Haskins SC (2007) Monitoring Anesthetized Patients. In: V. W. Lumb, E. W. Jones. Veterinary anesthesia and analgesia. 4th edn. Blackwell Publishing, Oxford, pp. 533-560.
- Keyes ML, Rush JE, Couto CG, Autran de Morais HS (1993) Ventricular Arrhythmias in Dogs With Splenic Masses. J Vet Emerg Crit Care 3, 33-38.
- Ko JC, Fox SM, Mandsager RE (2001) Effects of preemptive atropine administration on incidence of medetomidine-induced bradycardia in dogs. J Am Vet Med Assoc 218, 52-58.
- Laforcade AM (2010) Management of septic peritonitis in dogs and cats. In: Proceedings of the 35th World Small Animal Veterinary Congress. Geneva, Switzerland.
- Macintire DK (2006) Monitoring Critically Ill Cats and Dogs. In: Proceeding of the north american veterinary conference. Orlando, Florida, pp. 263-265.
- Mackenzie G, Barnhart M, Kennedy S, DeHoff W, Schertel E (2010) A Retrospective Study of Factors Influencing Survival Following Surgery for Gastric Dilatation-Volvulus Syndrome in 306 Dogs. J Am Anim Hosp Assoc 46, 97-102.
- Marino DJ, Matthiesen DT, Fox PR, Lesser MB, Stamoulis ME (1994) Ventricular arrhythmias in dogs undergoing splenectomy: a prospective study. Vet Surg 23, 101-106.
- Martin M (2007) Small animal ECGs: Introductory Guide. 2nd edn. Blackwell Publishing, Oxford.
- Mazzaferro E, Wagner AE (2001) Hypotension During Anesthesia in Dogs and Cats: Recognition, Causes, and Treatment. Compendium 28, 728-737.
- Moïse NS, Pariaut R, Gelzer AM, Kraus MS, Jung SW (2005) Cardioversion with lidocaine of vagally associated atrial fibrillation in two dogs. J Vet Cardiol 7, 143-148.
- Nolan J, Flapan AD, Capewell S, MacDonald TM, Neilson JM, Ewing DJ (1992) Decreased cardiac parasympathetic activity in chronic heart failure and its relation to left ventricular function. Br Heart J 67, 482-485.
- Oyama M (2015) Perioperative Monitoring of Heart Rate and Rhythm. Vet Clin North Am Small Anim Pract 45, 953-963.
- Papich MG (2016) Medetomidine Hydrochloride. In: M. G. Papich. Saunders Handbook of Veterinary Drugs. 4th edn. Elsevier, St. Louis, pp. 481-483.
- Peterson ME, Keene B, Ferguson DC, Pipers FS (1982) Electrocardiographic findings in 45 cats with hyperthyroidism. J Am Vet Med Assoc 180, 934-937.
- Pypendop B (2005) Monitoring of the respiratory system. In: 50th Congresso Nazionale Multisala. Rimini, Italia.
- Riordan LL, Schaer M (2009) Potassium Disorders. In: D. C. Silverstein, K. Hopper. Small Animal Critical Medicine. 1st edn. Saunders Elsevier, Toronto, pp. 229-232.
- Roux (2012) How I treat...Gastric Dilation and Volvolus (GVD). In: Proceedings of the Southern European Veterinary Conference and Congreso Nacional de AVEPA. Barcelona, Spain.
- Rowland E, McKenna WJ, Gulker H, Krikler DM (1983) The comparative effects of diltiazem and verapamil on atrioventricular conduction and atrioventricular reentry tachycardia. Circ Res 52, 163-168.
- Rudloff E, Raffe MR (2012) Arrhythmias in critical care. In: Proceeding of the Congreso Latinoamericano de Emergencia y Cuidados Intensivos. Mexico.
- Schober KE (2010) Medical Treatment of Tachyarrhythmias. In: Proceedings of the 35th World Small Animal Veterinary Congress. Geneva, Switzerland.
- Schwartz DS (2009) This dog has ventricular arrhythmias-what do I do? In: Proceedings of the 34th World Small Animal Veterinary Congress. Sao Paulo, Brazil.
- Silverstein D (2006) SIRS, MODS, and sepsis in small animals. In: International Congress of the Italian Association of Companion Animal Veterinarians. Rimini, Italy, pp. 107-108.
- Smith LJ (2002) Hypotension. In: S. A. Greene,Veterinary Anesthesia and Pain Management Secrets. Hanley & Belfus Inc, Philadelphia, pp. 135-140.
- Spyer KM (1994) Central nervous mechanisms contributing to cardiovasular control. J Physiol 474, 1-19.
- Stepien RL (2005) Cardiac arrhythmias: What to treat, when and how. In: Proceeding of the North American Veterinary Conference, Orlando, Florida.
- Tag TL, Day TK (2008) Electrocardiographic assessment of hyperkalemia in dogs and cats. J Vet Emerg Crit Care 18, 61-67.
- Tilley LP, Smith WFK (2016) Electrocardiography. In: L. P. Tilley,W. F. K. Smith, J. R. Smith, M. Oyama, M. Sleeper. Manual of Canine and Feline Cardiology. 5th edn. Elsevier, Toronto, pp. 49-77.
- Wendelburg KM, O’Toole TE, McCobb E, Price LL, Lyons JA, Berg J (2014) Risk factors for perioperative death in dogs undergoing splenectomy for splenic masses: 539 cases (2001-2012). J Am Anim Med Assoc 245, 1382-1390.
- William WM (2007) Cardiovascular system. In: V. W. Lumb, E. W. Jones. Veterinary anesthesia and analgesia. 4th edn. Blackwell Publishing, Oxford, pp. 61-116.
Υπεύθυνη αλληλογραφίας:
Ζωή Τζενετίδου
e-mail: Αυτή η διεύθυνση ηλεκτρονικού ταχυδρομείου προστατεύεται από τους αυτοματισμούς αποστολέων ανεπιθύμητων μηνυμάτων. Χρειάζεται να ενεργοποιήσετε τη JavaScript για να μπορέσετε να τη δείτε.



